国外研究团队开发了一种新的光学成像技术——编码光片阵列显微术(CLAM),它可以高速进行3D成像,并且具有足够的功率效率和柔和度,能够在扫描过程中以现有技术无法达到的水平保存活体标本。
数十年来,科学家一直在使用荧光显微镜来研究生物细胞和生物的内部运作。但是,这些平台中的许多平台通常太慢,无法跟随3D的生物学作用,并可能在强光照射下对生物样本造成破坏。
为了应对这些挑战,由香港大学(HKU)电气与电子工程学系副教授兼生物医学工程学学士学位课程主任、项目负责人Kevin Tsia博士领导的研究团队开发了一种新的光学成像技术——编码光片阵列显微术(CLAM)。它可以高速进行3D成像,并且具有足够的功率效率和柔和度,能够在扫描过程中以现有技术无法达到的水平保存活体标本。
Kevin Tsia博士(右一)和他的团队开发了一种新的光学成像技术,可以使3D荧光显微镜更高效,更不损坏。
这项先进的成像技术最近发表在《光:科学与应用》上,这项创新已经提交了美国专利申请。
新光学成像技术——编码光片阵列显微术(CLAM)
现有的3D生物显微镜平台速度较慢,因为必须依次扫描标本的全部体积,并逐点、逐行或逐平面成像。在这些平台上,单个3D快照需要在标本上重复照明,标本的光照强度通常是日光的数千倍至百万倍,这很可能会损坏标本本身,因此不利于长期用于各种解剖学、发育生物学和神经科学等领域的生物成像。
此外,这些平台通常很快耗尽有限的荧光“预算”——这是一个基本限制,即荧光灯只能在有限的时间内通过照明产生,然后在一个称为“光漂白”的过程中永久消失,这就限制了在一个样本上可以执行多少图像采集。
编码光片阵列显微镜(CLAM) 香港大学
Tsia博士说:“ 样品上的重复照明不仅会加速光致漂白,而且还会产生过多的荧光,最终无法形成最终图像。因此,荧光'预算'在这些成像平台上被大大浪费了。而CLAM允许以高帧速率进行3D荧光成像,与最先进的技术(每秒约10倍的体积)相当。更重要的是,它比科学实验室中广泛使用的标准3D显微镜更节能,比标准3D显微镜温和1000倍以上,这大大减少了扫描过程中对活体标本造成的损害。”
据介绍,CLAM的核心技术是使用一对平行反射镜将单个激光束转换成高密度的“光片”阵列,以荧光激发的方式将其扩散到整个样品区域。
整个3D体积内的图像可以同时(即并行化)拍摄的,而无需按其他技术的要求逐点、逐行或逐平面扫描样本。这样的CLAM中的3D并行化可产生非常柔和而有效的3D荧光成像,而不会牺牲灵敏度和速度,CLAM在降低光漂白效果方面也胜过普通的3D荧光成像方法。
同时,为了在CLAM中保持图像分辨率和质量,团队转向了码分复用(CDM),这是一种图像编码技术,已广泛应用于电信领域,用于同时发送多个信号。
开发该系统的另一位博士后研究员Queenie Lai博士解释说:“这种编码技术使我们能够使用2D图像传感器同时捕获和数字重建3D中的所有图像堆栈。CDM以前从未在3D成像中使用过,我们采用了这项技术,并取得了成功。”
作为概念验证的演示,该团队应用CLAM以每秒超过10体积的体积速率捕获微流体芯片中快速微粒流动的3D视频。
挑战极限 提高CLAM扫描速度
CLAM对成像速度没有根本的限制,唯一的限制来自系统中使用的检测器(即用于拍摄快照的相机)的速度。随着高速相机技术的不断发展,CLAM始终可以挑战其极限,以达到更高的扫描速度。
该团队进一步采取了行动,将CLAM与HKU LKS医学院新开发的组织清除技术相结合,以高帧频对小鼠肾小球和肠血管系统进行3D可视化。
使用CLAM进行3D高速成像。学分:香港大学
蔡医生说:“我们预计,这种组合技术可以扩展到档案生物学样本的大规模3D组织病理学研究,例如在大脑中绘制细胞组织以进行神经科学研究。由于CLAM成像比其他所有方法都要温和得多,因此它独特地有利于对生物样本以其活体形式进行长期和连续的'监视'。这可能会影响我们对细胞生物学许多方面的基本了解,例如不断跟踪动物胚胎发育成成年形式;实时监测细胞/生物如何被细菌或病毒感染;观察癌细胞如何被药物杀死,以及当今现有技术无法实现的其他挑战性任务。”
CLAM可以通过最少的硬件或软件修改就适用于许多当前的显微镜系统。利用此优势,该团队计划进一步升级当前的CLAM系统,以进行细胞生物学、动植物发育生物学研究。
-
光学成像
+关注
关注
0文章
87浏览量
10078 -
3D成像
+关注
关注
0文章
98浏览量
16056
发布评论请先 登录
相关推荐
裸眼3D笔记本电脑——先进的光场裸眼3D技术
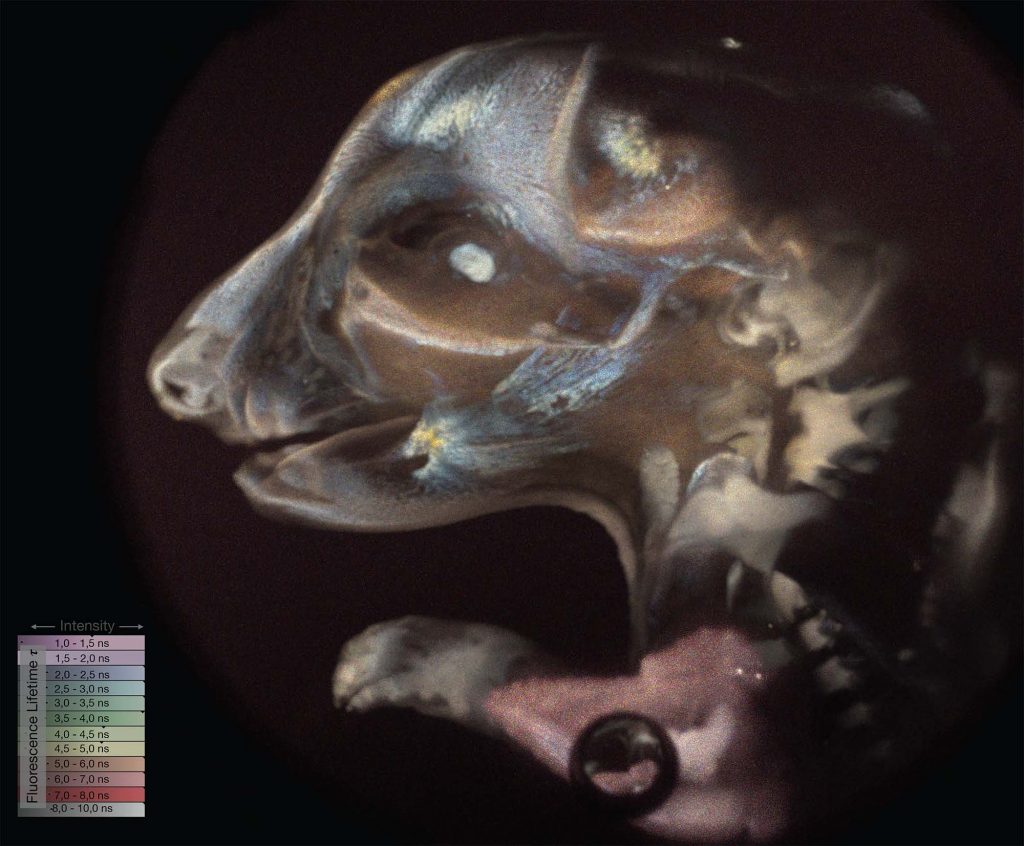
光片寿命成像
奥比中光3D相机打造高质量、低成本的3D动作捕捉与3D动画内容生成方案
微观特征轮廓尺寸测量:光学3D轮廓仪、共焦显微镜与台阶仪的应用
微观特征轮廓尺寸测量:光学3D轮廓仪、共焦显微镜与台阶仪的应用

什么是光场裸眼3D?

天马微电子首发TIANMA META SIGHT光场3D解决方案

显微测量|光学3D表面轮廓仪微纳米三维形貌一键测量
显微测量|共聚焦显微镜大倾角超清纳米三维显微成像
显微测量|光学3D表面轮廓仪微纳米三维形貌一键测量





 编码光片阵列显微术提高3D成像速度
编码光片阵列显微术提高3D成像速度












评论