制药业是大企业,但通常不被认可的大部分是具有复杂供应链,精细化学工艺和产品且必须满足严格质量控制要求的制造业。业内很少有人考虑如何安全,有效,大规模地以可靠的质量和精确计量的剂量来生产药物。
更有趣的是,简单的事实是,制药厂经常使用已经过时数十年的制造工艺来生产复杂的药物,并且在可比较的行业(例如化学制造)中正在逐步淘汰这种工艺。使用物联网传感器数据和预测性维护进行实时资产管理对于制药行业的成功和革命至关重要。
批处理过程和过渡困难
药品通常采用分批处理的方式生产,包括将化合物在大桶中混合,然后长时间拖延以测量每种中间产品的质量,然后进行下一步,有时在另一家工厂进行。机械不能连续使用。有关条件,状态和质量的信息通常分布在各种各样的独立系统中。仍收集一些关键数据并将其存储在纸质日志中。
如果制造过程是连续的,并用于从汽车到化学工业的各个方面,则制造效率会更高,在这种情况下,化合物可以不间断地在工厂内移动,并经过测试和测量,从而发挥了物联网的优势。连续制造还可以更灵活地响应需求。如果需要更多,您可以运行更长的时间来逐步增加产品,而随着批次的增加而增加数量则需要开始一个全新的批次,这意味着所有的延迟和供过于求的可能性。
不幸的是,在制药业实现现代化生产工艺的途径并非一帆风顺。
法规驱动的行业
考虑到药品制造中错误的可能后果,对药品进行了严格的监管。这些法规帮助延迟了制造流程,现在将推动变革。
当美国食品药品监督管理局(FDA)批准药品时,批准的不仅是活性化合物。包括制造过程本身的详细信息(包括工厂布局)。过程中的任何更改都需要获得相关文件工作的明确监管批准。在其他行业中,持续的流程改进,更快的库存访问和步骤的取消是公司竞争优势的一部分。制药业转型需要更多的计划。
FDA已经认识到固有的监管困难,并成立了新兴技术团队(ETT),其目的是鼓励采用新的制造方法,尤其是连续制造。目的是在任何法规提交之前,他们将在开发的早期与制药公司会面。任何提议的制造过程都将在提交批准之前进行全面审查。
尽管FDA对全球药品批准产生巨大影响,但它远非唯一一家此类机构。全球有100多个药品监管机构,全球制药商在计划更改生产流程时必须考虑到每个机构。
早期的成功
ETT已经证明了其有效性。自2015年以来,Vertex一直在为囊性纤维化药物Orkambi使用连续生产。经过漫长的开发周期,Janssen(现为强生公司的一部分)于2016年转向其HIV药物Prezista的连续生产。两者都与FDA密切互动,以确保在将药物提交批准之前批准了制造过程。强生特别指出,结合以前由物联网传感器实现的单独测试和采样步骤是一项重大改进。
合规优势
物联网在合规性方面的优势可能是其业务案例的重要组成部分,因为物联网提供了监视和记录制造过程中每个步骤的所有事件,变化和集中度的能力。从物联网传感器收集的数据使工厂操作员可以了解整个过程中发生的情况。如果某种化合物的特定运行与某种问题有关,这也可以为召回提供复杂的跟踪。
物联网还允许监视和记录承包制造组织(CMO)的活动,这些活动执行大部分实际制造。药物供应链变得越来越复杂,其中活性药物成分(API)的制造,整体配方和包装通常在不同的地方进行,通常由不同的签约供应商进行。
因此,药品监管机构对监控,跟踪和报告的需求可以推动物联网的采用并降低其速度。法规遵从性是经常被低估的IoT驱动程序。
物联网与制药业的发展之路
制药设备及其组成成分往往非常昂贵,并且制造条件必须保持在极窄的公差范围内。连续制造将使生产线上任何地方设备故障的后果更加严重。批处理可以在一个地方或另一个地方等待一会儿,这使得单点设备故障显得更为宽容。使用物联网传感器数据和预测性维护进行实时资产管理至关重要。
除了停产线的成本外,还有保持质量的问题,这是FDA最重要的考虑因素。他们总是犯谨慎的一面,所以任何可能引起质量问题的药物都是有罪的,直到被证明是无辜的。因此,预计故障,基于磨损的更换以及最少的计划外停机时间将使管理制造质量,效率和法规遵从性变得更加容易,同时还能灵活地适应不断变化的市场需求。
责任编辑:YYX
-
物联网
+关注
关注
2914文章
45014浏览量
377944 -
FDA
+关注
关注
0文章
76浏览量
18404
发布评论请先 登录
相关推荐
宇树科技在物联网方面
王老吉药业能源数字化管控系统项目顺利验收


浅谈安科瑞EMS2.0能效管理平台在制药厂洁净室的电气设计与选型
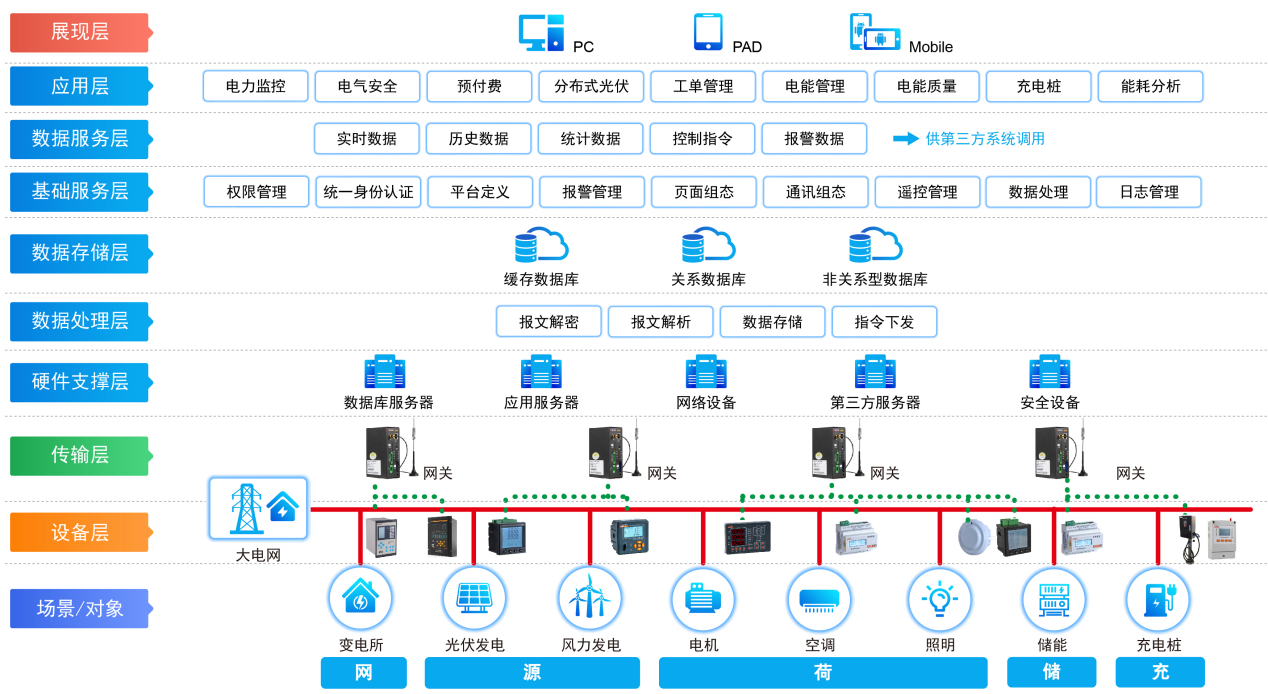
什么是物联网技术?
“物联网+农业”助力农业节水增效高质量发展
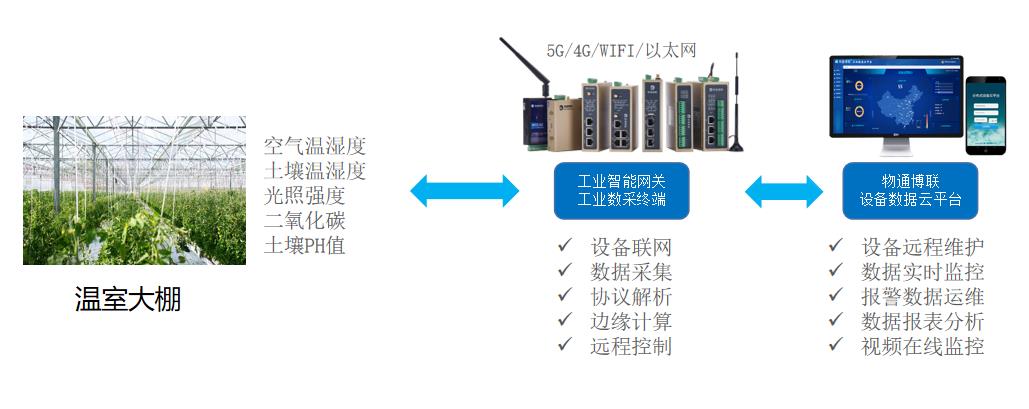
4G物联网开关求助
以创新驱动农业可持续发展之路,共谋发展新篇张





 物联网与制药业的发展之路
物联网与制药业的发展之路










评论