近年来,可开关微腔激光技术的发展大幅增强了光与物质的相互作用并在集成光子学领域具有重要应用。通常可开关微腔激光通过改变激光腔内部微纳米结构或折射率来实现切换,相对繁琐,变化性也小。
与人工制造的界面相比,刺激响应性的生物界面具有可利用生物系统和生物识别的优势,从而实现更高级的功能并可定制多种纳米级光学响应。除此之外,可开关的生物界面通常是指对生物分子相互作用响应后改变其微观性质的界面。尽管刺激响应性的生物界面在光电应用上已取得了很大的进展,具有生物识别的可开关微腔激光尚未获得突破性进展,特别是在宽波长范围内实现波长的可逆性和可调性方面。
DNA是人类和其他活生物体所有细胞核中的遗传物质。除了在生物学中的意义外,DNA在控制许多物理设备方面也发挥了特定作用。人们利用特定的DNA碱基配对来控制光与物质的相互作用已有一定的历史,但并未有人将之整合到法布里-珀罗微腔中控制激光发射,如图一。
图1 激光随着DNA结构在法布里-珀罗微腔内的变化而改变输出信号
图源:新加坡南洋理工 Yu-Cheng Chen课题组
针对以上问题,可参考新加坡南洋理工大学电机与电子工程学院Yu-Cheng Chen教授课题组:“利用有机生物分子DNA碱基配对形成具有生物识别的特性,实现了可开关微腔激光。”
这是利用生物分子控制激光的革命性进展。该成果证实了激光信号可以精准被生物分子控制的可能性,未来将应用于信息传输与编程。该研究工作以“DNA Self-Switchable Microlaser”为题在线发表在ACS Nano。
法布里-珀罗微腔包含两个反射镜和在两镜之间的光学增益介质。课题组采用掺了染料的液晶为增益介质,目的是为了增强对碱基配对的响应,并利用DNA-液晶特殊的互动,作为转换原理来改变微腔中液晶的排列方向从而实现激光中不同波长之间的切换。
由于熵的原因,单链与双链在液体中的结构不同。单链DNA(sDNA)通常以纠结的松弛形式存在。碱基配对后DNA产生构象变化,形成相对刚性的双链DNA(dsDNA)。
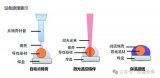
如图二所示,作者预先将液晶定向(垂直于镜子)。当注入的sDNA被液晶表面的正电荷吸引而嵌入液晶时,液晶开始改变排列方向与镜子平行。液晶表面的单链DNA杂交成双链时,液晶的排列则恢复到垂直方向。
图2 DNA分子与液晶的交互作用,激光可以有效地在时域上变换输出不同发光波长
图源: 新加坡南洋理工 Yu-Cheng Chen课题组
在本文中,利用激光腔的DNA碱基配对,研究人员发现:
1. 当单链DNA (ssDNA)注入时,激光波长出现蓝移。
2. 如果注入与ssDNA互补的另一条单链DNA(cDNA),经过生物自我辨识,两条单链DNA杂交形成双链,激光波长红移。
3. 除了波长的位移,激光的时间强度也随DNA的嵌入发生变化,仿佛液晶随着DNA跳圆舞曲一般。
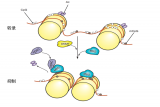
在此微腔中,增益介质是由掺杂染料与液晶形成的主-客体复合材料。液晶的永久性偶极矩产生作用于染料的诱导偶极矩。因此染料的排列也会随着液晶而改变。如图三所示。 当入射光的电矢量(E)垂直于染料分子的主轴时,会发生弱吸收。当入射光的电矢量(E)平行于染料分子的主轴时,会发生强吸收。在注入了sDNA的F-P腔中加入cDNA之前和之后的激光切换。碱基开始配对后,激光开始返回原始波长附近。
图3 DNA 激光切换波长的机制与原理 (先蓝移,结合后又红移回去)
图源:新加坡南洋理工 Yu-Cheng Chen课题组
作者分别从入射光的偏振、增益介质的折射率、染料的吸收强度和荧光发射强度分析了液晶的排列对增益介质的影响。实验和理论研究均表明,增益介质的吸收强度随着液晶排列变化,是决定激光位移的关键机制。
总结这项研究的意义在于引入使用有机生物分子切换不同波长相干光源的概念。该团队认为,DNA特定分子识别的非凡能力将来可能会适合诸如激光的信息编码和数据存储之类的应用。通过利用DNA的自我识别和序列的复杂性,可以对激光进行完全的操纵和编程。这项研究通过利用生物分子的复杂性和自我识别,为亚纳米级可编程光子器件的开发提供了启示。
文章信息
DNA Self-Switchable Microlaser, ACS Nano 2020.
本文的通讯作者为新加坡南洋理工大学电机与电子工程学院Yu-Cheng Chen教授, 第一作者为课题组博士后张艺凡,该工作与太原理工大学王文杰教授合作。
责任编辑:PSY
-
激光
+关注
关注
19文章
3212浏览量
64562 -
DNA
+关注
关注
0文章
243浏览量
31059 -
光子学
+关注
关注
0文章
37浏览量
11371 -
微纳米
+关注
关注
0文章
18浏览量
7576
发布评论请先 登录
相关推荐
不同锡丝的激光焊锡使用
kvm切换器怎么实现键盘热键切换
激光焊接工艺有哪些?
DNA计算机研究取得突破性进展:PB级数据存储与高效处理
FSC中高压无扰动周波快速切换系统 双电源快切柜 介绍

激光测距仪如何改成速度计
电源切换开关芯片怎么接
电源切换芯片怎么设置
激光焊接机在塑料领域的应用

无缝高清矩阵切换器和传统的矩阵切换器有什么区别?
基于Transformer的多模态BEV融合方案
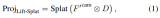




 DNA与激光的融合和切换
DNA与激光的融合和切换










评论