背景:随着医疗器械行业迅速发展,新技术和新产品日新月异、层出不穷,给人民大众提供了更好的健康保障,但与此同时,医疗器械不良事件也频频发生。采用医疗器械唯一标识(UDI)可以很好地解决这个问题。UDI可实现医疗器械从生产、加工到流通、配送、使用全流程的溯源和监管。
医疗器械唯一标识由产品标识和生产标识组成,产品标识是识别注册人/备案人、医疗器械型号规格和包装的唯一代码,是从数据库获取医疗器械相关信息的“关键字”,是唯一标识的必需部分;生产标识包括与生产过程相关的信息,包括产品批号、序列号、生产日期和失效日期等,可与产品标识联合使用,满足医疗器械流通和使用环节精细化识别和记录的需求。
基于GS1标准的UDI编制结构包括器械标识静态信息DI、生产标识动态信息PI。其中,DI包括全球贸易项目代码GTIN,具体有包装指示符、厂商识别代码、商品项目代码、校验码等。PI具体包括应用标识符、有效期、序列号、生产日期等。由于医疗器械使用风险和监管追溯要求的不同,其器械的唯一标识也会随之变化。UDI可由DI单独表示,也可由DI加PI联合使用表示。根据不同的医疗器械产品,可标识到规格型号、批次、单品。
所有产品UDI码都是现场生成,由现场工控平台上传至UDI追溯后台。关键点:保证每一台工控平台生成的码都不重复。
分页机分页→系统控制喷码机在产品上赋UDI码→在线检测UDI码是否可读→能读取的进行自动收集→不能读取的报警和自动剔除处理→生产的产品数据上传到UDI追溯平台。
医疗器械实施UDI之后能带来什么好处?
1、能简化将器械使用信息集成到数据系统的操作;
2、能快速识别出现不良事件的医疗器械;
3、能更快速地为已报告的问题制定对应解决方案;
4、能够减少医疗差错;
5、提供更迅速、有效的器械召回解决方案;
6、实现突出重点且有效的药监部门安全沟通;
7、可以轻松访问准确器械标识信息的原始来源。
UDI是医疗器械的唯一身份证,为每个医疗器械赋予身份证,实现生产、经营、使用各环节的透明化、可视化,提升产品的可追溯性,是医疗器械监管手段创新和监管效能提升的重要标志。
fqj
-
医疗器械
+关注
关注
19文章
823浏览量
51442 -
数据库
+关注
关注
7文章
3799浏览量
64375
发布评论请先 登录
相关推荐
医疗器械中电磁干扰的来源及影响

如何编制有源医疗器械设计开发流程?

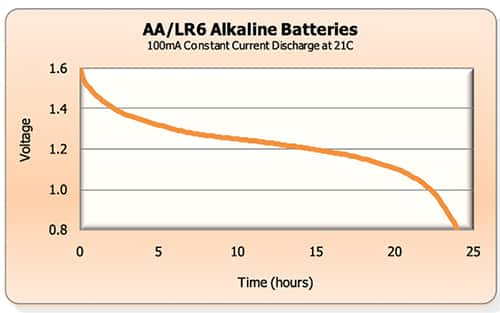
选择和优化医疗器械中的电池


FMEA在医疗器械风险分析中的应用
1000+医疗器械新质生产力企业汇聚Medtec 2024

上海国际医疗器械展览会2025年6月25日-27日举办
医疗器械密封性负压测试仪评估





 UDI医疗器械唯一标识系统:身边的UDI专家
UDI医疗器械唯一标识系统:身边的UDI专家














评论