基因疗法作为一种可以实现治疗性蛋白的长期表达和组织特异性表达的治疗方法,可以实现治疗传统药物不能治疗的疾病,或大幅改善治疗疾病的方式。甚至面对很多先天性遗传的疾病时,基因疗法是许多患者唯一的希望。
基因疗法在技术上获得实践可能,离不开2012年CRISPR/Cas9技术的发现,“CRISPR”即“Clustered Regularly Interspaced Short Palindromic Repeats”,是细菌遗传密码及其免疫系统的一个定义性特征,是细菌用来保护自己免受病毒攻击的防御系统。
实质上,它是一系列重复的DNA序列,并且这些DNA之间存在“spacers”。简而言之,细菌利用这些基因序列来“记住”攻击它们的每种病毒。细菌会将病毒的DNA整合到自己的细菌基因组中。这种病毒DNA最终成为CRISPR序列中的“spacers ”。这种防御系统可以在同种病毒再次发起攻击时给予细菌保护或免疫力。
总是位于CRISPR附近的基因,称为Cas(CRISPR相关)基因。一旦激活,这些基因就会产生特殊的蛋白质,这些蛋白质是与CRISPR共同进化的酶。这些Cas酶能够充当切割DNA的“分子剪刀”。
简单来说,当病毒侵入细菌时,其独特的DNA会被整合到细菌基因组中的CRISPR序列中。这意味着下一次病毒攻击时,细菌会记住它并发送RNA和Cas来定位和破坏病毒。
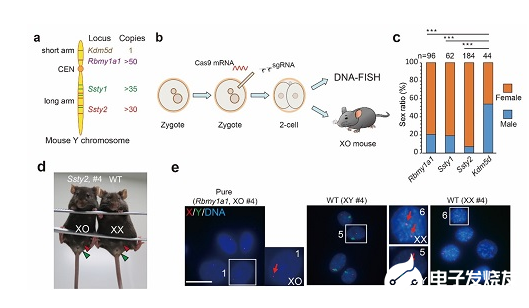
虽然细菌中还有其他Cas酶在病毒攻击自己时会截断病毒,但Cas9是动物体内执行这种任务的最佳酶。而CRISPR-Cas9就是指切割动物(和人类)DNA的Cas酶的种类。
因此,CRISPR/Cas9系统也被视为基因疗法的剪刀。近日,约翰霍普金斯大学医学院(Johns Hopkins Medicine)的研究人员,在一种常见细菌中,找到了CRISPR-Cas9系统工作原理的新线索,为开发新的Cas9工具带来重要的指导意义。
和人类的免疫系统一样,细菌的免疫系统也需要保持平衡:在识别和消除威胁时需要提高活性,同时要适时调低活性以便错误地攻击细菌自己。其中,科学家们发现,CRISPR-Cas9系统中有一种RNA分子(tracrRNA),会导致该系统的活性急剧增加。这种tracrRNA分子像支架一样,帮助Cas9携带向导RNA切断特定的DNA序列。
tracrRNA有长、短两种形式,它们结构相似,也都可以与Cas9结合。科学家们发挥CRISPR-Cas9的“基因剪刀”功能时,用的是短链tracrRNA。而在这项研究中,科学家们揭示了长链tracrRNA不曾被发现的功能。
研究人员发现,长链tracrRNA包含了一个模拟向导RNA的片段,但不同于向导RNA靶向病毒DNA序列,长链tracrRNA倾向于靶向CRISPR-Cas9系统本身。
而且,当它结合到特定位置时,并没有让Cas9剪切DNA,而是待在那里阻碍基因的表达。而当研究人员人为改变长链tracrRNA中某个区域的长度后,随着长度的改变,Cas9可以恢复切割活性。
在另一组实验中,研究人员培养了具有大量长链tracrRNA的细菌,CRISPR相关基因的表达量则非常低。而从中除去长链tracrRNA后,CRISPR-Cas9基因的表达量增加了100倍。
这意味着,长链tracrRNA其实是在抑制自身CRISPR相关的活性,而长链tracrRNA调节基因活动将为未来设计新型CRISPR-Cas9工具提供更多机会。
责任编辑:PSY
-
DNA
+关注
关注
0文章
243浏览量
31157 -
基因
+关注
关注
0文章
95浏览量
17257 -
免疫系统
+关注
关注
0文章
13浏览量
7311
发布评论请先 登录
相关推荐
亚马逊云科技发布Amazon Bedrock新功能
Amazon Q Business新功能发布,助力企业提效
Amazon Q Business发布新功能 助力企业提升内部工作效率
解析NVIDIA JetPack 6.1的新功能

首批Apple Intelligence功能惊艳亮相,12月新功能值得期待
NVIDIA Parabricks v4.3.1版本的新功能
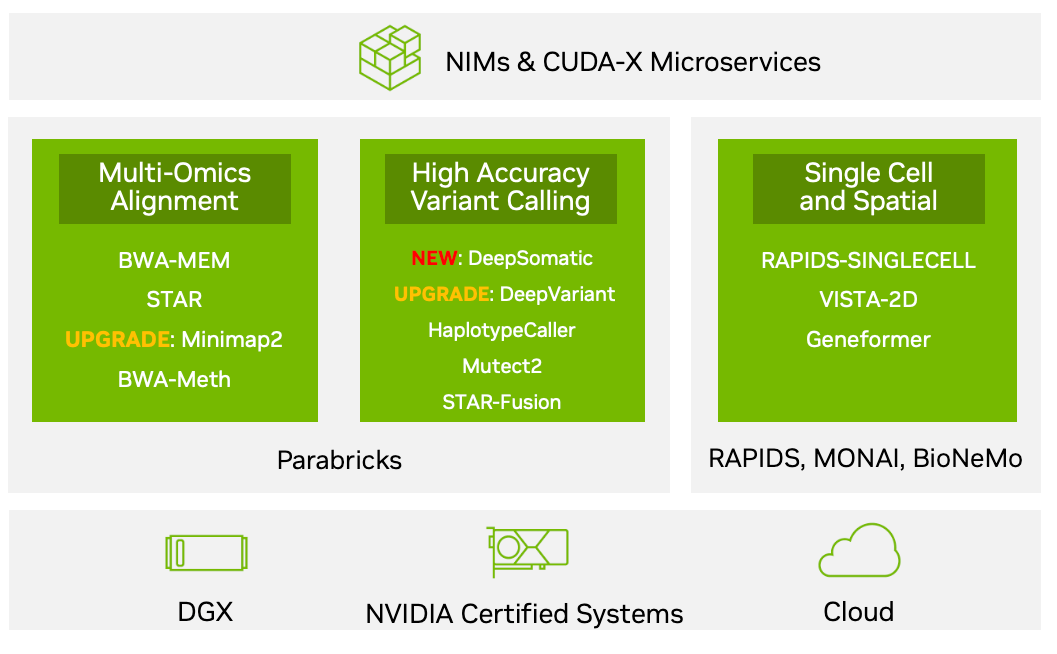




 基因“剪刀”新功能 提供更多机会
基因“剪刀”新功能 提供更多机会











评论