自2019年12月以来, 全球流行的严重急性呼吸综合征冠状病毒2(SARS-CoV-2)已感染过亿人,并导致了近2500万人死亡。现在全球报告的新型冠状病毒肺炎(COVID-19)病例数已经连续五周下降,表明即使存在病毒变体,简单的公共卫生措施(大规模筛查和主动隔离)仍能发挥作用。对于大规模筛查而言,需要高灵敏、高通量和低成本的检测方法以识别感染者和追踪潜在感染者,改善局部控制能力,并为区域疾病控制工作提供依据。RT-qPCR方法是COVID-19诊断的金标准方法,却受限于训练有素的人员和昂贵的仪器需求,而无法在欠发达国家和地区广泛应用。因此亟需快速、灵敏、无需专业人员操作和复杂设备的COVID-19高通量测试方法以扩展COVID-19的诊断能力。
近来,美国杜兰大学医学院分子诊断中心的胡晔教授和宁波教授报道了一种基于CRISRP技术的超灵敏、高通量COVID-19荧光诊断系统(CRISPR-FDS, CRISPR-based fluorescent detection system)。相关研究以“Ultra-sensitive and high-throughput CRISPR-powered COVID-19 diagnosis”为题发表在国际权威期刊杂志《Biosensors and Bioelectronics》上(DOI:10.1016/j.bios.2020.112316)。南昌大学博士研究生黄震为该论文的第一作者。
研究的主要内容介绍
CRISPR-FDS利用一步RT-PCR技术扩增从样品提取的病毒RNA目标片段(ORF1ab 和N基因),将所得的扩增子整体转移至基于gRNA/Cas12a的CRISPR系统中进行荧光检测。目标特异性的gRNA将引导Cas12a蛋白特异性切割目标基因,同时非特异性切割单链荧光探针以释放荧光信号。该方法也兼容RPA等恒温扩增技术,可将检测时间缩短至50分钟。CRISRP-FDS于其他非SARS-CoV-2病原体无交叉,且检测限低至2 拷贝/反应,较RT-qPCR优势明显。且与临床实验室进行RT-qPCR测试相比,针对同样的COVID-19疑似病例鼻拭子样本进行测试,CRISRP-FDS方法表现出更高的灵敏度和稳定性。
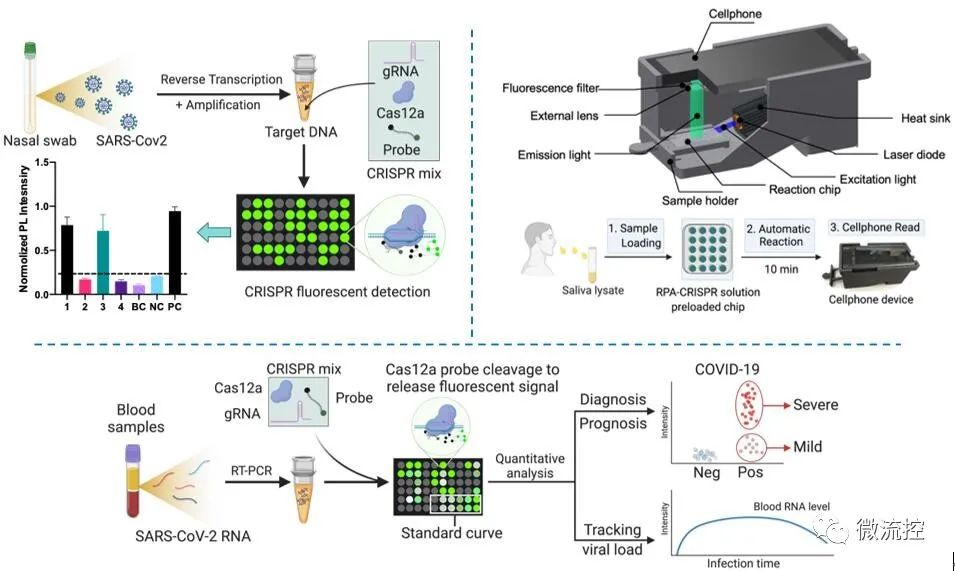
CRISPR-FDS 诊断流程。该方法兼容拭子,唾液和血液等多种标本,即可应用于大规模筛查,也可实现POCT检测,且具有极大的临床应用潜力。
值得注意的是,CRISPR-FDS采用了大多数临床实验室中容易获得的试剂和设备,可以很容易地实现自动化,以满足对高通量测试的需求。而且,胡教授团队进一步整合CRISPR-FDS技术和微流控芯片技术,实现了基于智能手机读取的唾液POCT测试(Science advances, DOI: 10.1126/sciadv.abe3703)以提升欠发达地区的测试能力。另外,胡教授团队基于CRISPR-FDS技术定量追踪感染者血液中的病毒RNA,临床研究表明该技术可以改善COVID-19诊断,用于SARS-CoV-2感染清除的评估,并预测感染的严重程度(Journal of Clinical Investigation, DOI: 10.1172/JCI146031)。
小结
CRISPR-FDS具有超高的灵敏度和特异性,简单,稳定且无需昂贵的仪器,适用于COVID-19的大规模筛查。基于该技术的唾液POCT测试可以进一步扩展其应用场景,提升欠发达地区的检测能力。而且临床验证已经表明,CRISPR-FDS具有重大的临床应用价值以评估SARS-CoV-2的清除和预测疾病严重程度。
责任编辑:lq
-
微流控芯片
+关注
关注
13文章
270浏览量
18829 -
荧光检测
+关注
关注
0文章
7浏览量
6531 -
COVID-19
+关注
关注
0文章
226浏览量
10536
原文标题:生物传感器:CRISPR驱动的超灵敏高通量COVID-19诊断
文章出处:【微信号:MEMSensor,微信公众号:MEMS】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
诊断系统开发咨询服务
高通量生物分析技术之微流控芯片
智能开关柜故障诊断系统如何实现?
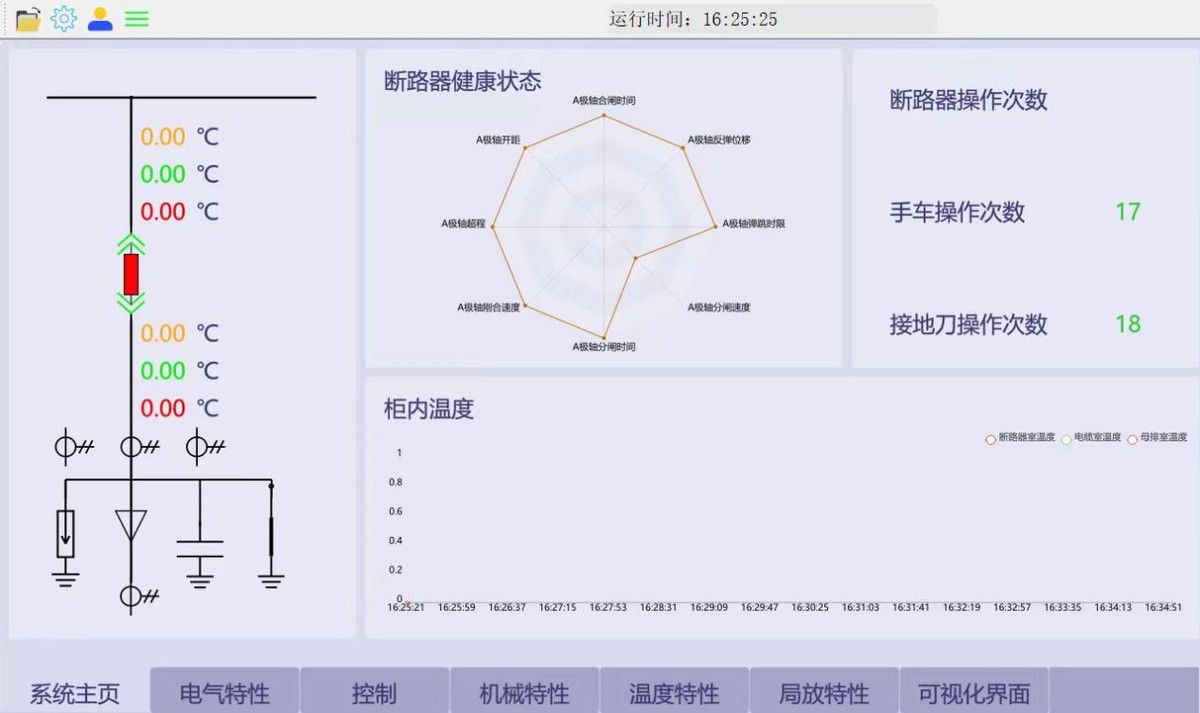
输电线路故障不再愁,输电线路故障智能诊断系统来帮忙

光伏电站故障预警与在线监测智能诊断系统 一键运检 多维度故障对比
智能开关设备专家诊断系统平台的介绍
中置式开关柜技术规范:智能开关专家诊断系统

TPIR 785 高通量高灵敏度拉曼光谱仪

闪光科技高灵敏超快成像及燃烧诊断技术交流会在西北工业大学成功举办

中国移动浙江公司携手华为完成5G-A高通量UPF全球现网首呼
赋能产业互联网,高通量计算让世界更高效!





 一种基于CRISRP技术的超灵敏、高通量COVID-19荧光诊断系统
一种基于CRISRP技术的超灵敏、高通量COVID-19荧光诊断系统











评论