Implandata公司的可植入式青光眼生物传感器Eyemate-SC曾于今年4月获得了FDA突破性设备认定(Breakthrough Device Designation),近日通过CE Mark认证。
据麦姆斯咨询报道,眼科产品公司Implandata将其Eyemate-SC生物传感器与Eyemate系统相结合,用于青光眼数字化远程监测和管理。这款可植入式青光眼生物传感器,在获得FDA批准后数周后通过CE MARK认证,正式获准在欧盟上市。
Implandata表示,该专利系统是首批临床验证的用于青光眼综合远程监测的产品之一。4月获得美国FDA(美国食品和药品管理局)突破性设备认定(Breakthrough Device Designation,BDD)。
突破性设备认定仅适用于对有可能危及生命或使人衰弱的不可逆转的疾病,提供更有疗效的突破性技术,以便在不危及安全的情况下,使患者和医生更及时地获得此类技术。
据Implandata创始人兼首席执行官Max G. Ostermeier介绍,按照FDA突破性设备认定计划推进,意味着公司产品将从上市前的开发期间、提交过程以及提交后的快速审查期间,得益FDA的额外投入。
他说:“随着FDA的市场授权,目前,Eyemate系统将有权享受至少4年的创新技术医疗保险(Medicare Coverage of Innovative Technology),为受益人提供可预见的突破性Eyemate系统访问权限,帮助他们改善健康。”
Implandata表示,该系统是其前身产品的升级版本。每天全天监测的眼压(intraocular pressure,IOP)数据,可以帮助主治医生根据患者的特定需求定制青光眼药物。
Ostermeier还指出,微创传感器作为公司验证的Eyemate系统的一部分,通过CE MARK(欧盟标志)认证,是公司向青光眼护理转型迈出的重要一步。
Ostermeier在一份声明中说:“这个新版本正在扩大可寻址青光眼患者群体,比以前的器件植入更容易、更安全。有了CE MARK,我们将在欧洲各地的眼部中心推出该产品。”
该器件可帮助患者自行测量眼压,收集到的信息会自动实时发送给他们的眼科医生或进行云存储。这些信息使眼科医生获得关于治疗效果的详细信息,并根据患者的当前状况调整治疗,而不是仅根据就诊期间获得的单次眼压测量值进行调整。
加州大学圣地亚哥分校(University of California, San Diego)眼科主席兼特聘教授、Implandata医学顾问、医学博士Robert N. Weinreb指出,全球有数百万人因青光眼而面临永久性失明的风险。
他在一份声明中说:“通过Eyemate,可以更密切地监测眼压,以实现个性化治疗,避免视力进一步恶化。”
瑞士洛桑Clinique de Montchoisi眼科顾问医师、科罗拉多大学丹佛分校(University of Colorado, Denver)眼科学系副教授、公共卫生硕士、医学博士Kaweh Mansouri,是验证生物传感器临床研究的主要研究人员之一。
他在一份声明中说:“Eyemate-SC生物传感器已通过CE Mark认证,现在我们可将Eyemate系统引入常规临床,这是我们此前热切期待的。我们团队对该产品在临床研究中表现出的安全性和性能非常满意,同时很高兴患者对该产品较好的接受程度。”
此外,Mansouri指出,Eyemate将帮助眼科医生更快地做出更明智的治疗决定。
他总结说:“这项技术增强了患者的治疗信心,提高了治疗依从性,减少了患者对并未发生的高眼压峰值和青光眼加重的担忧。”
编辑:jq
-
数字化
+关注
关注
8文章
8763浏览量
61836 -
生物传感器
+关注
关注
12文章
370浏览量
37389 -
FDA
+关注
关注
0文章
76浏览量
18333
原文标题:用于青光眼远程护理的生物传感器Eyemate-SC获准上市
文章出处:【微信号:Micro-Fluidics,微信公众号:微流控】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
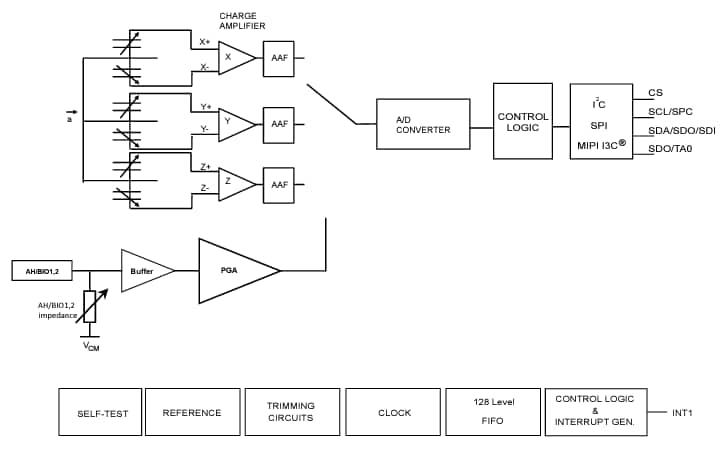
意法半导体推出超低功耗生物传感器ST1VAFE3BX
生物传感器:科技前沿的生物监测利器
#新品# ST1VAFE3BX生物传感器(带vAFE)
高可调性材料:Haydale生物传感器油墨,打造灵活定制化印刷解决方案
Aigtek功率放大器如何帮助纳米电子生物传感器更好的研发和生产
思特威全新推出图像传感器产品SC521PC及SC200PC
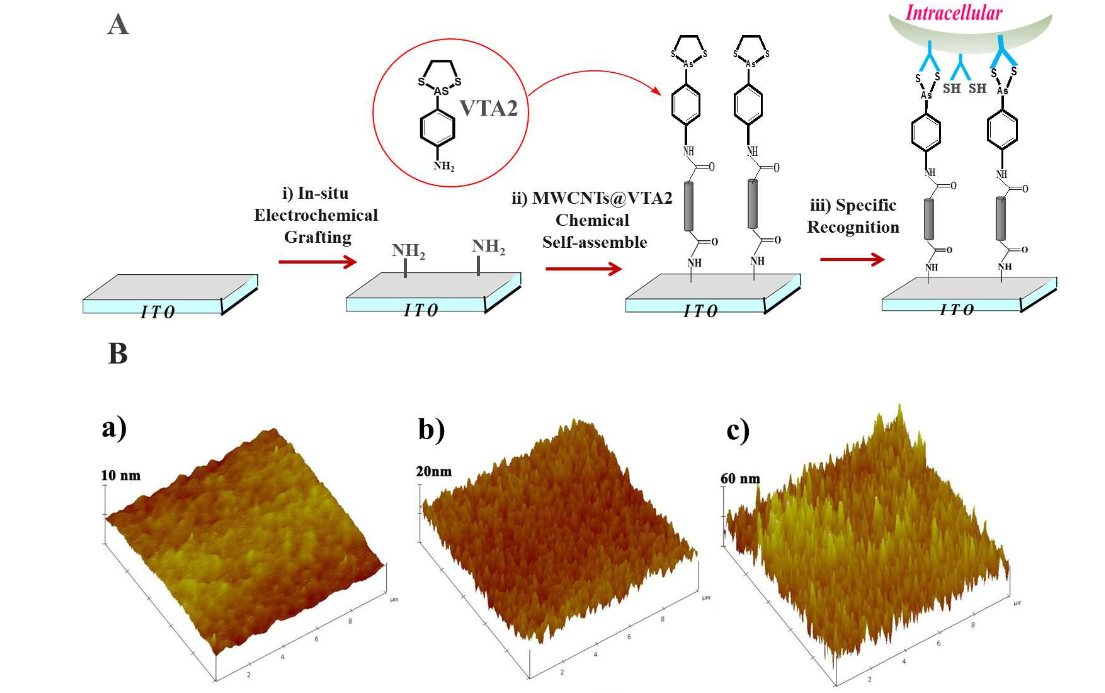
电化学生物传感器在生物检测领域的显著优势
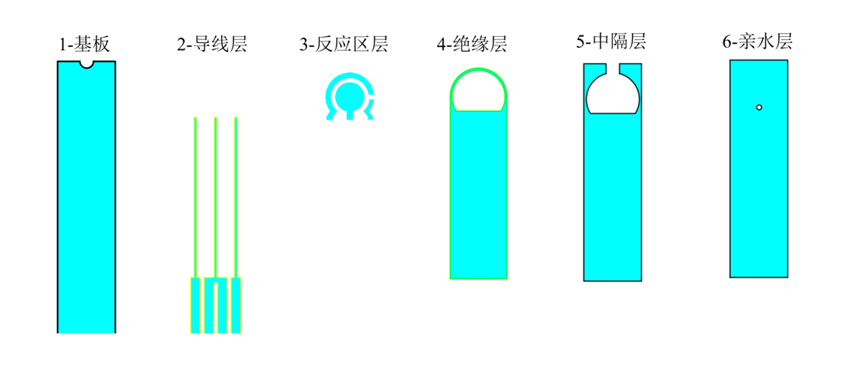
便携快速检测的电化学生物传感器:颠覆性变革生物检测方式
生物医学领域的传感器有哪些?
安泰ATA-2161高压放大器在生物传感器研究中的应用
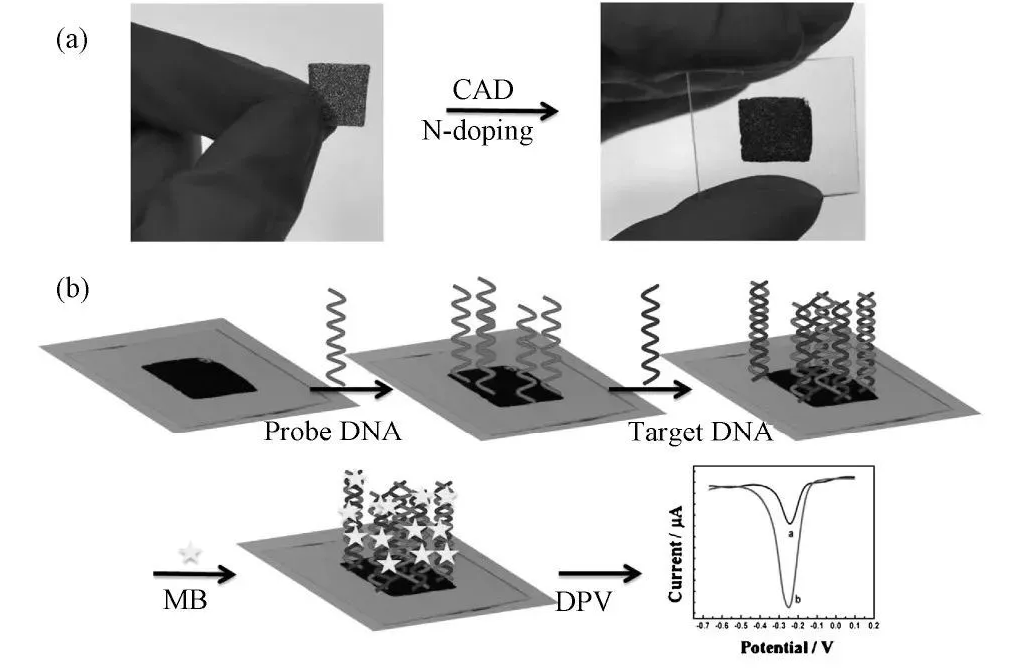
用于原位监测汗液标志物的全打印、多模态可穿戴生物传感器阵列
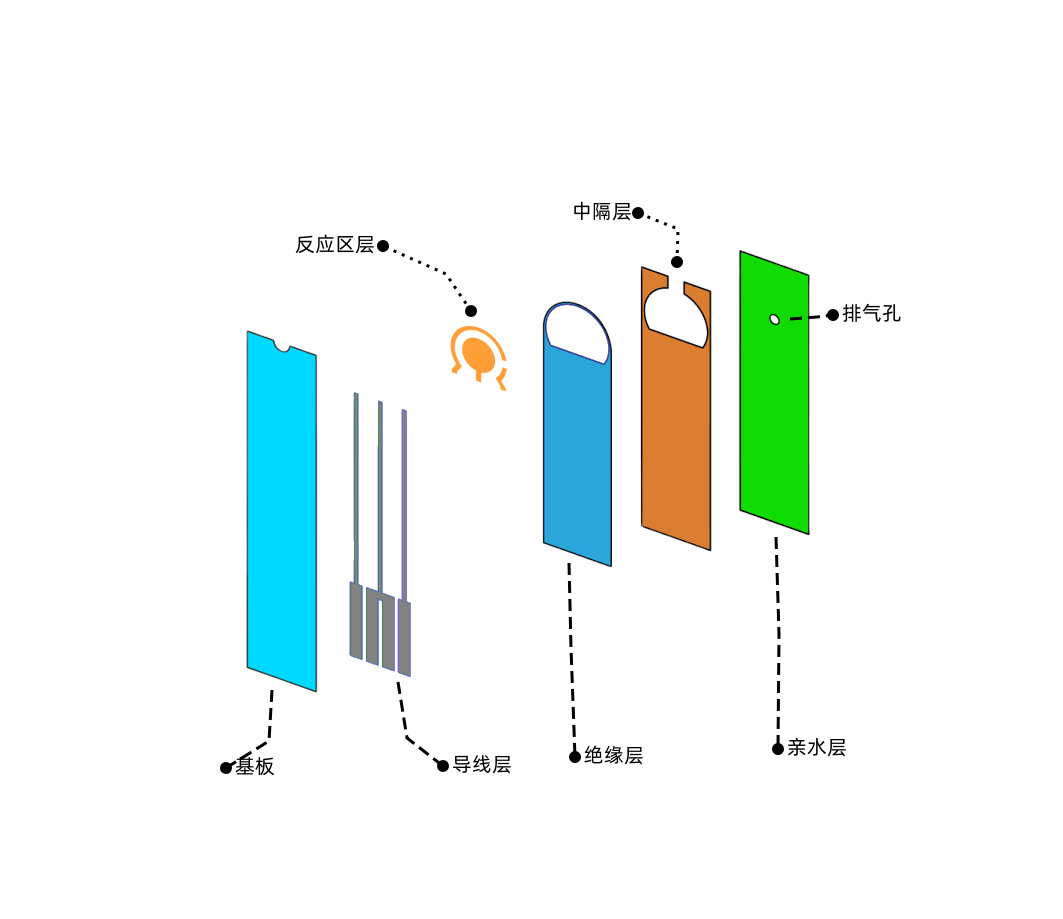
科普|生物传感器
思特威推出5000万像素图像传感器SC5000CS





 Implandata推出用于青光眼远程护理的生物传感器Eyemate-SC获准上市
Implandata推出用于青光眼远程护理的生物传感器Eyemate-SC获准上市










评论