化石能源的过度开采和利用导致严重的环境问题和能源危机。可再生能源驱动的电催化二氧化碳还原产生液态燃料和化学物质,有效的实现碳中和能源转化。在众多的还原产物中,甲酸盐是二氧化碳电化学还原具有市场竞争力和经济可行性产物,开发高效电催化二氧化碳还原产甲酸催化剂具有重要研究价值。目前,电催化二氧化碳还原转化体系主要耦合阳极氧析出反应(OER),OER能耗高、产物附加值低。因此,以热动力学有利的氧化反应代替OER耦合电化学二氧化碳还原,超低电压下实现高附加值产物的制备具有重大意义。本文亮点
1.在膜电极中,二氧化碳还原反应(CO₂RR)耦合甲醛氧化反应(FOR)实现了甲酸盐的成对电合成。
2.采用热力学更有利的甲醛氧化反应代替氧析出反应,降低能耗。
3. CO₂RR//FOR 展现出优异的电化学性能(100 mA cm⁻² @ 0.86 V), 甲酸盐质量归一化所消耗的电能为0.413 Wh g⁻¹。
内容简介
开发低槽压、高附加值的二氧化碳还原共电解体系具有重要意义。湖南大学邹雨芹教授等人采用热力学有利的甲醛电氧化耦合阴极二氧化碳还原,实现超低电压下甲酸盐的成对电合成。首先在H池分别评估BiOCl电催化二氧化碳还原及Cu₂O电催化甲醛氧化的性能,宽电压区间甲酸盐的法拉第效率均大于90%。此外,分别在H池、流动池及膜电极组装二氧化碳还原耦合甲醛氧化共电解体系,在膜电极中达到100 mA cm⁻²电流密度仅需要0.86 V,远低于大部分二氧化碳还原耦合小分子电氧化体系。低槽压、高附加值的甲酸盐成对电合成体系成功的构建表明甲醛电氧化代替氧析出反应具有广阔的应用前景。
图文导读
I催化剂的形貌及结构表征
电化学二氧化碳还原产甲酸盐的催化剂为BiOCl。XRD谱图证实BiOCl催化剂成功制备,BiOCl展现出光滑的表面,厚度大约为50 nm。Bi 4f XPS谱图表明BiOCl中Bi以Bi³⁺形式存在。
电化学甲醛氧化的催化剂为Cu₂O,首先用氧气等离子体处理泡沫铜正反两面各5 min, 然后在1 M KOH电解液进行原位电化学还原,-0.4 VRHE还原400秒。Cu俄歇LMM表明Cu以Cu⁺存在。Cu 2p分峰拟合的结果表明,原位电化学还原后Cu²⁺明显下降。
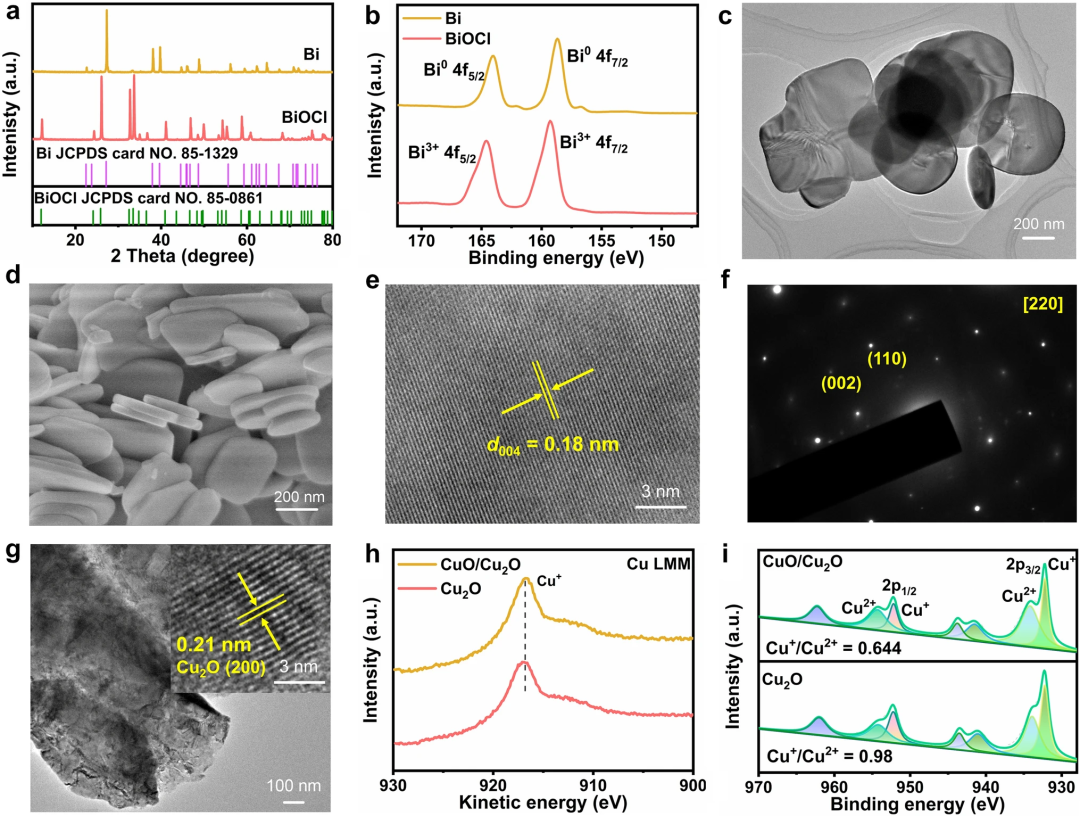
图1. 二氧化碳还原和甲酸氧化催化剂的形貌及结构表征。BiOCl和商业化Bi粉(a) XRD谱图,(b) Bi 4f谱图;BiOCl的(c) TEM,(d) SEM,(e) HRTEM,(f) SAED谱图;(g) Cu₂O的TEM 及HRTEM谱图;CuO/Cu₂O及Cu₂O (h) Cu俄歇LMM及(i) Cu 2p谱图。
II阴极CO₂RR电催化性能
电化学二氧化碳还原性能在H池测试。BiOCl及商业化Bi粉在CO₂饱和电解液极化曲线电流密度远高于Ar饱和0.5 M KHCO₃,表明铋基催化剂有利于二氧化碳还原反应而不是氢析出(图2a)。相比于商业化Bi粉,BiOCl展现出更优异二氧化碳还原产甲酸盐性能。同时,BiOCl具有优异稳定性及更小的电荷转移电阻。BiOCl电化学活性面积校正的甲酸盐局部电流密度远高于商业化Bi粉,BiOCl具有更高的本征活性。
流动池结合气体扩散电极打破二氧化碳传质的限制,提高了二氧化碳还原的反应活性。图3a为流动池的示意图。相比于H池,BiOCl在流动池电流密度得到了极大提高(图3b)。BiOCl在-0.48 ~ -1.32 VRHE电压区间具有较高的甲酸盐法拉第效率以及优异的稳定性。
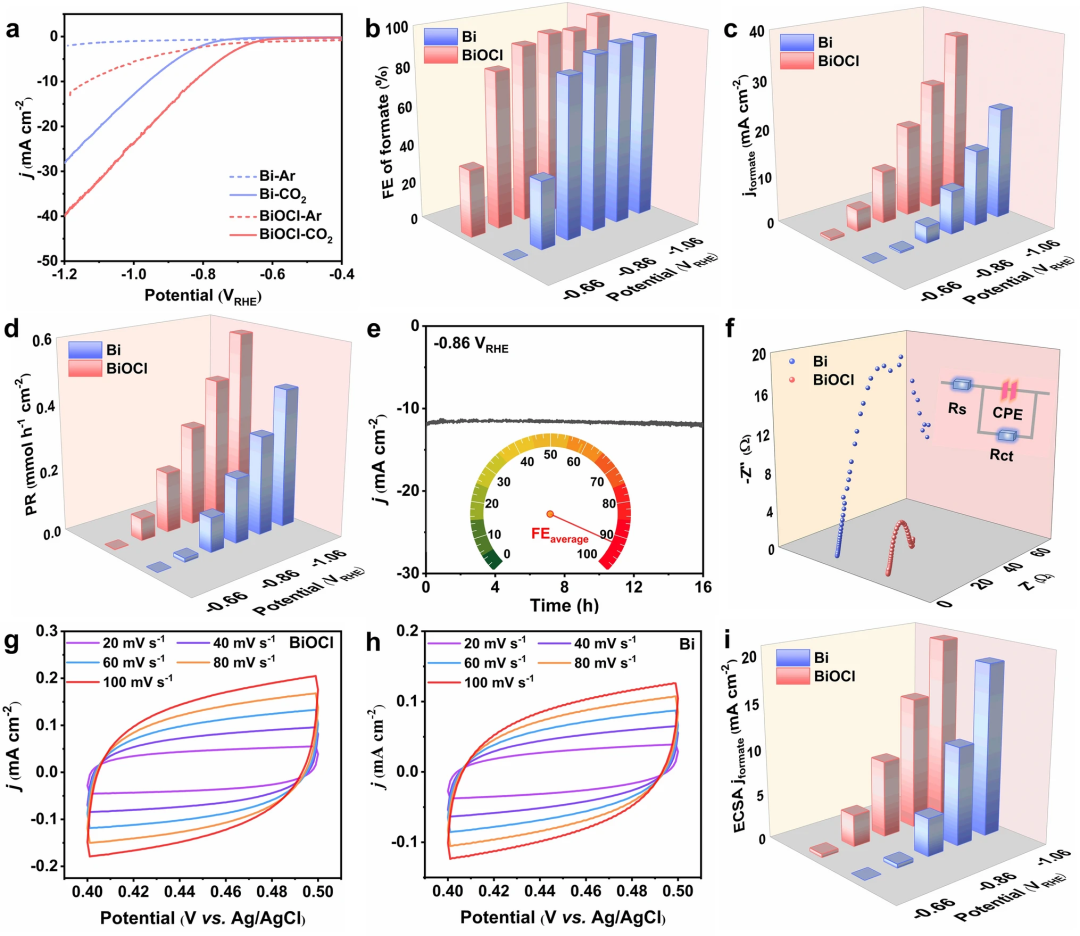
图2. 铋基催化剂在H池中阴极二氧化碳还原电化学性能。(a) BiOCl和商业化Bi粉在Ar或CO₂饱和的0.5 M KHCO₃电解液极化曲线;BiOCl和商业化Bi粉在不同电压下(b)甲酸盐的法拉第效率,(c)甲酸盐的局部电流密度,(d)甲酸盐的产生速率;(e) BiOCl在-0.86 VRHE进行16 h稳定性测试;(f) BiOCl和商业化Bi粉在-0.76 VRHE奈奎斯特图;(g) BiOCl和 (h)商业化Bi粉在不同扫速下的循环伏安曲线;(i)电化学活性面积校正的甲酸盐局部电流密度。
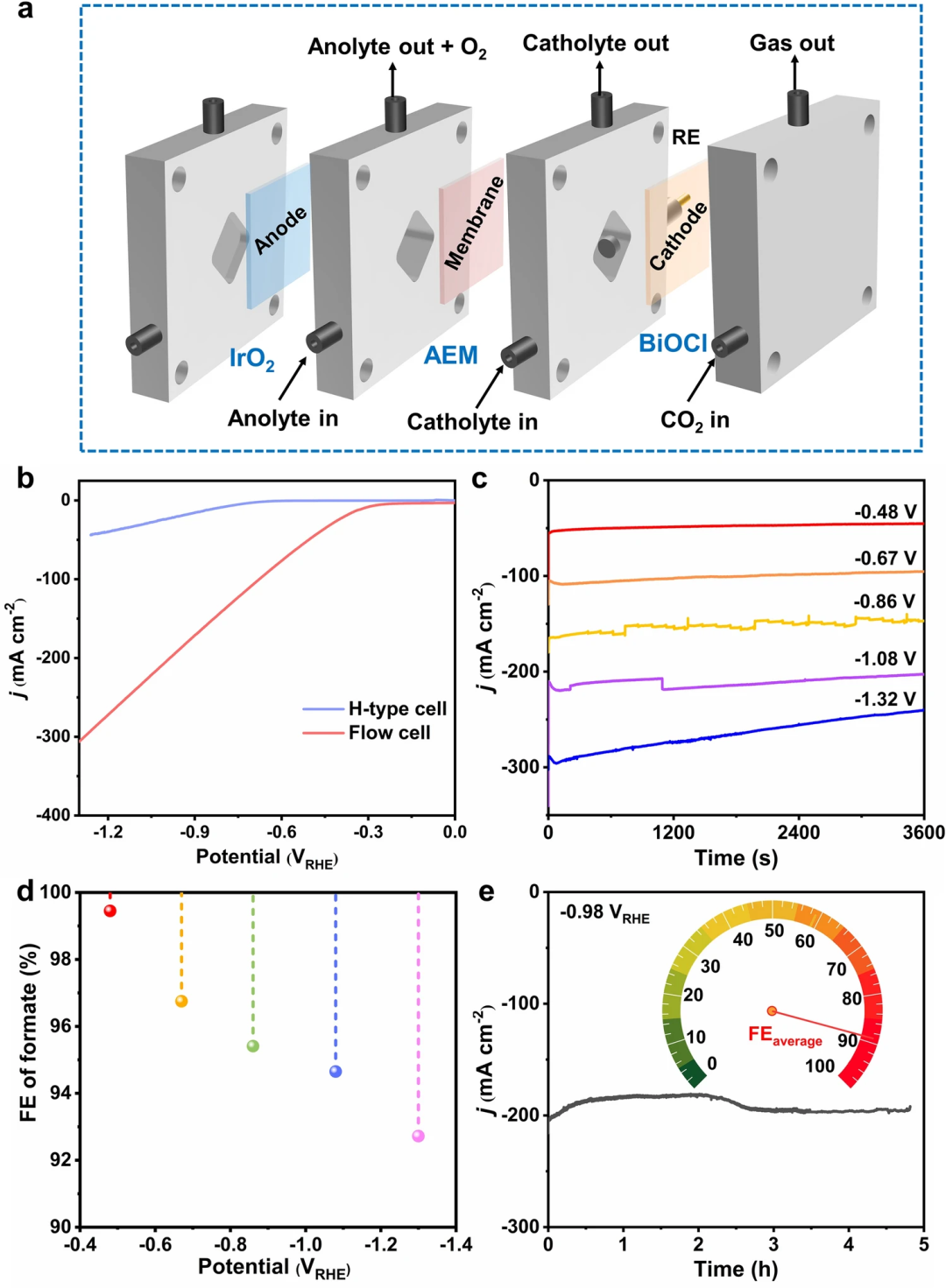
图3. BiOCl在流动池阴极CO₂RR电化学性能。(a) 流动池示意图;(b) BiOCl在H池和流动池的极化曲线;(c)恒电压电解,(d)电压依赖的甲酸盐法拉第效率从-0.48 ~ -1.32 VRHE;(e) BiOCl在流动池-0.98 VRHE稳定性测试。
III阳极FOR电催化性能
相比于氧析出反应,甲醛电化学氧化形成甲酸盐及氢气是热力学有利的反应,达到100 mA cm⁻²所需要的电压仅为0.238 VRHE(图4a)。在-0.05 ~ 0.35 VRHE电压区间电解直到甲醛完全转化,甲醛电化学氧化形成的甲酸盐浓度在0.25 VRHE达到最大值87.7 mM,还有10.1 mM甲酸盐来源于坎尼扎罗反应。随着电解电压的增加,甲酸盐的形成速率增加,0.35 VRHE甲酸盐的形成速率达到最大值1.48 mmol h⁻¹ cm⁻²。-0.05 ~ 0.35 VRHE电解区间,甲醛电氧化形成甲酸盐的法拉第效率均大于90%。Cu₂O在0.35 VRHE电压下进行连续6次电解测试,甲酸盐法拉第效率几乎均大于90%,证明催化剂具有优异的稳定性。甲醛电化学氧化后, Cu仍以Cu⁺形成存在,Cu⁺/Cu²⁺比例急剧上升,一部分Cu²⁺被还原为Cu⁺。

图4. (a) Cu₂O在含有/不含有甲醛1 M KOH电解液中极化曲线;(b) 甲醛电化学氧化所形成的甲酸盐浓度及甲酸盐总产生速率;(c) 不同电压下甲醛完全转化所形成的甲酸盐的法拉第效率;(d) Cu₂O进行连续6次电解循环所产生的甲酸盐法拉第效率;Cu₂O进行甲醛氧化前和甲醛氧化后(e) Cu俄歇LMM及(f) Cu 2p谱图。
IV二氧化碳还原耦合甲醛氧化电化学性能
甲酸盐成对电合成在膜电极进行组装,图5a为甲酸盐成对电合成的示意图。相比于H池,膜电极打破了二氧化碳传质的限制,缩短了阴极和阳极间的距离,降低了内阻。膜电极二氧化碳还原耦合甲醛氧化达到100 mA cm⁻²电流密度仅需0.86 V。在0.3 ~ 1.0 V槽压下电解,二氧化碳还原产甲酸盐及甲醛电氧化产甲酸盐的平均法拉第效率几乎均高于90%。1.0 V槽压下进行10 h稳定性测试,阴极二氧化碳还原和阳极甲醛电氧化产甲酸盐的平均法拉第效率之和高于190%。二氧化碳耦合甲醛氧化提供了一种新型而有效的方法实现超低电压甲酸盐的成对电合成。
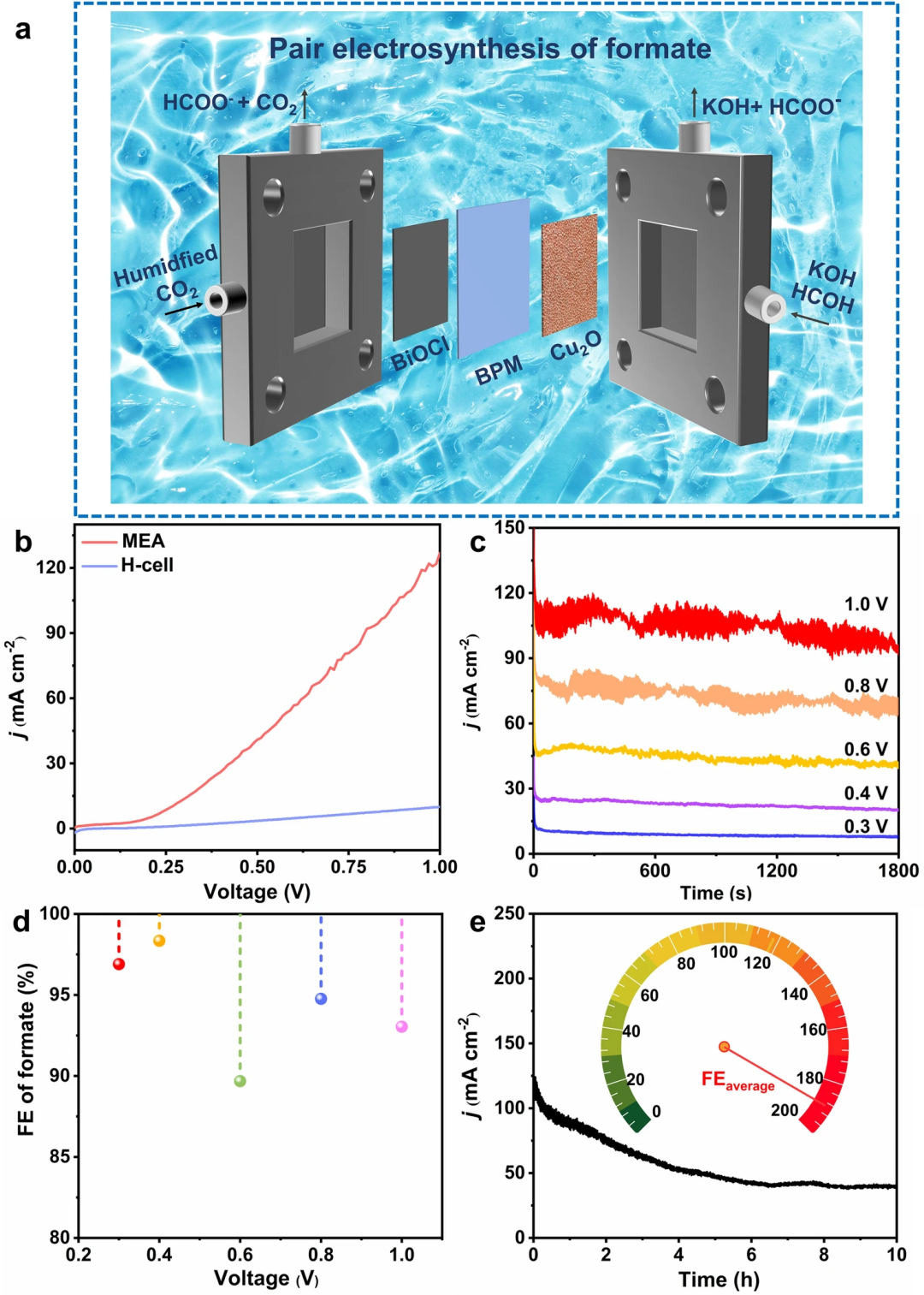
图5. 二氧化碳还原耦合甲醛氧化在膜电极的电化学性能。(a) CO₂RR//FOR在膜电极中示意图;(b) CO₂RR//FOR在H-池和膜电极极化曲线;(c) 恒电压电解,(d) 电压依赖的甲酸盐法拉第效率从0.3-1.0 V;(e) 在1.0 V进行10 h稳定性测试。
审核编辑:郭婷
-
电流
+关注
关注
40文章
7227浏览量
141591 -
可再生能源
+关注
关注
1文章
761浏览量
40745
原文标题:湖南大学邹雨芹NML:二氧化碳还原耦合甲醛氧化,在超低电压下电合成甲酸盐
文章出处:【微信号:清新电源,微信公众号:清新电源】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
国产红外二氧化碳传感器哪家强?全面对比分析
选择二氧化碳气体泄漏检测仪应注意什么?

探索XENSIV™ PAS CO2 1.5传感器:高精度二氧化碳检测的新选择
艾迈斯欧司朗与合作伙伴联合推出可大幅降低二氧化碳排放的纸质卷盘LED运输解决方案
双光路红外二氧化碳气体传感器:精准监测背后的技术革新

创新驱动与产业变革:超临界二氧化碳发电技术的差异化发展路径与前景展望

甲醛颗粒物温湿度等多合一检测设备

精准捕捉环境信号:二氧化碳 / 温湿度 / 光照度四合一传感器解析
无线数传模块在CO₂驱油中的高效无线通讯应用案例
尺寸虽小,内有乾坤: Sensirion突破性微型二氧化碳传感器发售

二氧化碳温湿度光照度传感器:四合一,在线监测气体
树莓派的可持续解决方案:年二氧化碳排放量减少了43吨!

呼气末二氧化碳监测中的传感器应用

二氧化碳光声传感技术




 二氧化碳还原耦合甲醛氧化实现高附加值产物的制备
二氧化碳还原耦合甲醛氧化实现高附加值产物的制备





评论