导 读
汽车运输的电气化和可再生能源整合是减少气体排放和全球变暖的两条重要途径。这些都带来了储能技术方面的挑战,为此,电池成为一种多功能、高效的选择。然而,锂离子电池的有限循环寿命限制了其在固定能量存储应用中的长期使用。为了实现锂离子电池更广泛的市场渗透,需要详细了解其老化机理。老化被定义为系统性能、寿命和可靠性的降低,电池老化可能会导致其容量衰减或功率衰减或二者兼有。典型的锂离子电池由电极活性材料、粘结剂、导电剂、隔膜、集流体和电解质组成,这些部件之间的相互作用对电池的成功运行起着关键作用。因此,这些部件的老化及其导致的性能恶化会影响其他部件,进而加速整个电池系统的老化。锂电池的主要老化机制及其相互作用的示意图如图1所示,展现了锂离子衰减机制的复杂性。本文将详细分析电池不同部件发生的副反应,描述电池的老化特性并揭示相应的老化机制。
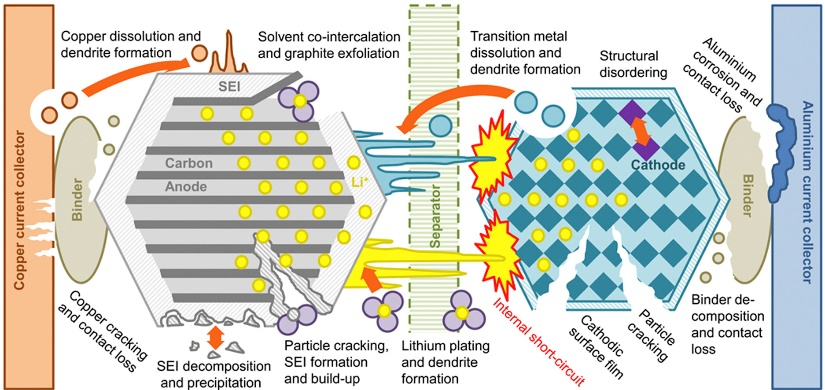
图1 锂离子电池的老化机理示意图[1]
1.阳极的老化机理
1)SEI膜的形成及稳定增长
许多研究人员认为,石墨阳极上的主要老化因素是在阳极表面的固体电解质界面(Solid electrolyte interphase,SEI)变化[2, 3]。如图2所示,SEI膜在电极表面附近形成,以保护阳极免受可能的腐蚀,并防止电解质在首次充电期间减少[4, 5]。然而,SEI是不稳定的,因为锂离子电池经常在电解质的电化学稳定范围之外工作。因此,SEI增长在电池寿命期间持续发生,这导致活性锂的消耗和电解质的分解。活性锂的消耗导致电极阻抗增加,电池容量和功率衰减。与SEI形成的初始阶段相比,由于分解反应动力学或溶剂分子扩散的限制,SEI以较低的速率生长[6]。这意味着SEI在增长的过程中相对稳定,而且容量损失在短期内并不显著,这允许锂离子电池的长期使用。锂离子电池的使用条件,包括高电压、高SOC和高温,都会加剧上述过程。电池在高电压水平下储存时,溶剂分子会通过SEI扩散后与石墨相互作用,可能导致石墨剥落和气体生成,从而造成SEI膜的开裂。在高SOC下,较低的阳极电势加速了上述副反应[7]。高温将降低SEI的稳定性和电极循环性能,因为SEI的溶解和溶剂分子的共插入被加强,进而产生对锂离子渗透性较低的锂盐,从而导致电极阻抗的增加[8]。
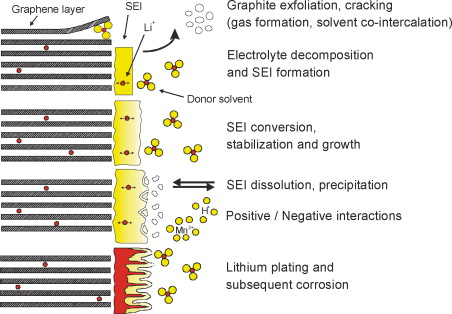
图2 SEI膜的变化过程[9]
2)锂沉积和锂枝晶的形成
一旦电极-电解质界面处的锂离子浓度超过电解质的饱和极限,石墨阳极的表面就会发生锂金属沉积[10]。除了活性锂消耗导致的容量损失外,锂沉积过程中锂枝晶的形成还可能导致隔膜撕裂及随后的短路和电池瞬间失效[3]。高电流、低温和高SOC可使阳极表面上的锂离子量达到引发锂枝晶所需的临界锂离子量[11, 12]。高电流会带来更高的极化效应,这意味着石墨表面的锂离子数量会增加从而堆积在阳极表面。此外,低温和高SOC下,锂的插层动力学减慢,增加了枝晶形成的可能性。枝晶形成的过电位在很大程度上取决于石墨表面的特性、温度、枝晶表面积和锂离子浓度。由于在阳极表面形成的枝晶的表面积会连续增加,所以一旦锂枝晶开始形成,枝晶形成的过电位会迅速降低。此外,由于锂沿着表面的扩散,在表面上的扭结和台阶处的锂离子的量局部高于正常表面平面。因此,在缺陷处锂沉积的概率更高[13, 14]。图3说明了锂枝晶的形成过程。由于锂的不均匀沉积带来的阳极中的应力导致枝晶晶须变形。如果沉积锂的量限制了锂离子通过电极-电解质界面的扩散,则进入的锂离子开始沉积在晶须的尖端以及扭结点[15]。锂在石墨上的沉积是部分可逆的。在高阳极电位下,仍与集流体有电气连接的活性锂可以再次溶解成锂离子。然而,若活性锂被SEI膜完全包覆、失去和石墨的电气连接,活性锂将成为死锂。因此,部分锂枝晶被隔离并广泛分布,造成锂枝晶的树枝状生长和死锂的扩散。这一过程可能导致内部短路,甚至热失控,对电池的安全性构成威胁。
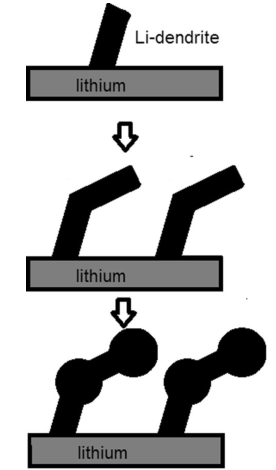
图3 锂枝晶的形成过程[16]
3)活性材料结构的变化
在电池性能退化过程中,活性材料内部通常会发生轻微的老化效应,表现为石墨有序结构的破坏。当锂电池以高速率循环时,由于锂离子浓度的梯度差异,在活性材料中产生机械应力场,导致阳极晶格的变化,从而导致阳极的初始分层结构的无序[17]。由于锂离子和电解质反应的无序颗粒之间存在新的界面,锂离子更难嵌入石墨中[18, 19]。因此,活性材料结构变化导致可逆容量的降低。此外,溶剂共插、石墨中的电解质还原和石墨中的气体沉淀导致的石墨颗粒开裂和石墨剥落将导致活性物质的损失,加速阳极降解[3, 4]。
4)阳极结构的变化
石墨材料的粒径尺寸对阳极性能有很大影响。小颗粒材料可以缩短石墨材料之间的扩散路径,这有利于高速充电/放电。然而,小颗粒材料具有更大的比表面积,这将在高温下消耗更多的锂离子,导致阳极的不可逆容量增加。因此,活性材料的粒径尺寸与阳极的热稳定性有关[20]。活性材料的体积变化也是接触损失的原因之一,碳颗粒、碳和集电体、碳和粘合剂以及集电体和粘合剂之间可能发生接触损失,导致电池的内阻增加[9]。此外,活性材料的体积变化对电极的孔隙率具有负面影响。石墨电极的孔隙率与阳极的可逆容量有一定的关系。随着孔隙率的增加,电解质更容易渗透到阳极中,从而使石墨和电解质之间的接触面积增加。石墨和电解质之间界面反应的增加导致可逆容量的降低。高压固体密度石墨电极具有低孔隙率,这可以延迟阳极的老化。
2.阴极的老化机理
1)活性材料的溶解
活性材料溶解引起的衰减主要存在于LMO阴极中,特别是在高温、高电荷状态和低电势下[21, 22]。在LMO正极材料中,锰通常处于两种氧化态,即Mn3+和Mn4+,其中Mn3+不稳定,可能溶解为Mn2+和Mn4+。Mn3+是固体结构,而Mn2+会溶解在电解质中,这导致与活性材料损失相关的容量衰减[23]。同时,电解液中H2O和LiF6结合形成的HF也可能导致锰的酸溶解,并在电极表面形成不溶性LiF,从而导致电极阻抗增加。对于腐蚀的阴极,晶体结构被破坏,导致锂元素的存储位置减少,容量衰减。对于具有低电势阳极(如锂化碳基阳极)的电池,溶解的锰离子将穿过隔板并沉积在阳极表面和/或催化SEI增稠反应,这导致锂库存损失和阳极内阻增加[24]。
2)阴极结构的变化
锂离子在正极材料中的插入/提取过程导致材料体积的变化。体积的膨胀/收缩导致活性材料颗粒以及电极中产生机械应力和应变。这种结构变化对阴极性能的影响大于碳基阳极[9]。此外,这种脱嵌过程会导致阴极氧化物的相变,从而扭曲晶格结构[21]。一些相变是可逆的,比如LiFeO4与FePO4在循环过程中两相共存;但也有一些不可逆的相变会导致晶格结构坍塌,从而导致容量损失,如图4所示,由于相反过渡金属层中氧原子的排斥相互作用,层状氧化物在脱锂状态下变得不稳定。特别是当电池过度充电时,大量锂离子从阴极中提取,导致材料的严重相变和结构的坍塌。
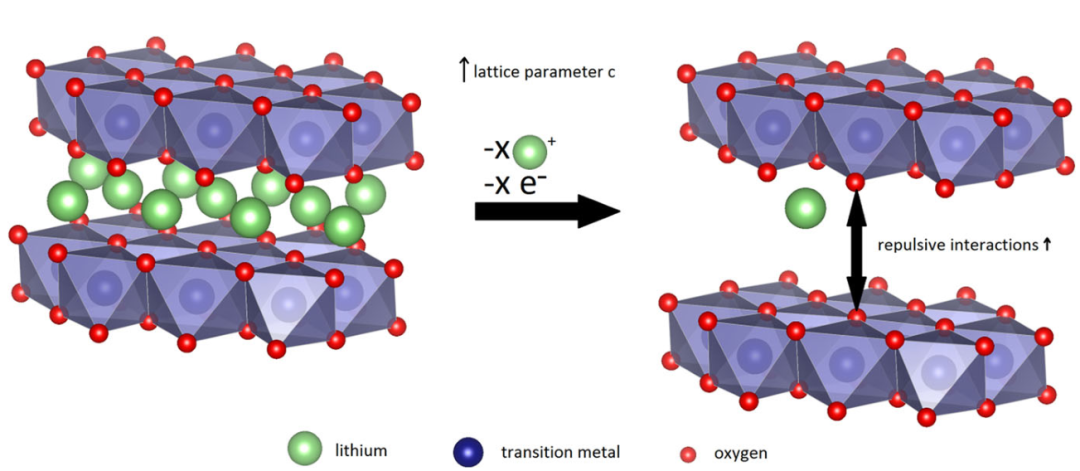
图4脱锂时的层状锂-过渡金属氧化物[15]
充放电引起的循环应力也会导致电极材料晶体结构的无序(图5)。新的晶体结构可能会导致锂离子被困在结构中,以及锂离子存储位置的损失。这两种效应都会导致容量衰减。且电池在高电压或高电流下的长期循环将导致阴极材料开裂。如果裂纹分布在阴极内部,由于与电解质缺乏接触,Li+的扩散将受到阻碍,这可能会导致一些阴极材料处于“隔离”状态。此外,裂纹还将导致阴极结构的不稳定性,并进一步导致阴极材料的粉化和塌陷。
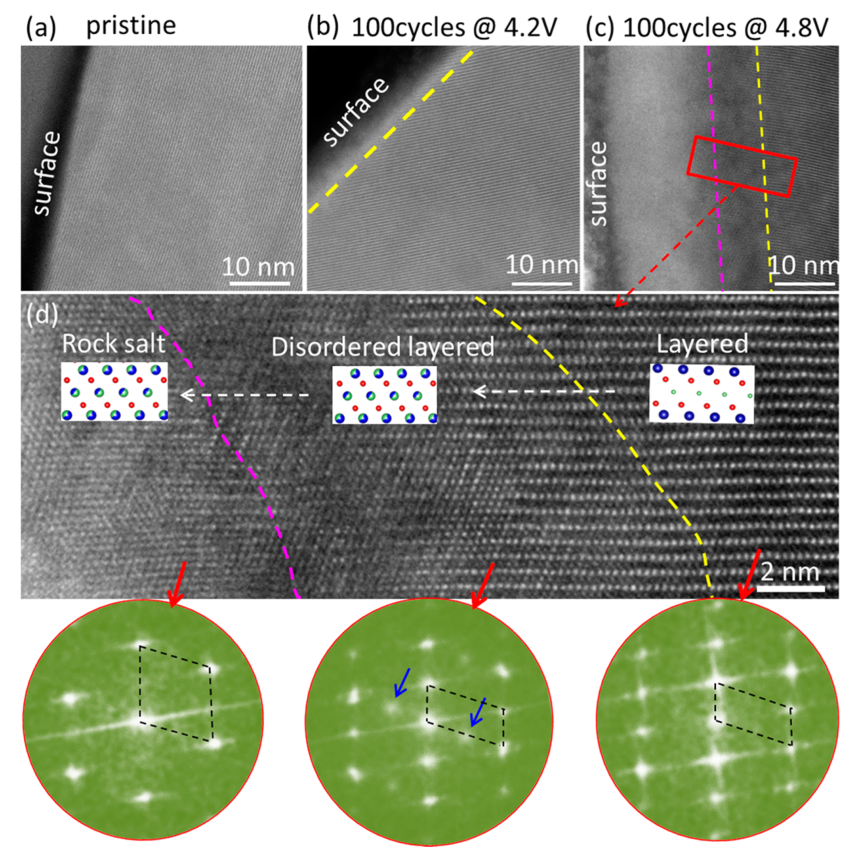
图5 NMC333阴极表面层的STEM-HAADF图像。(a)未经循环的原始样品。(b)在具有4.2V的高截止电压的100次循环之后(c)在具有4.8V的高切断电压的100个循环之后(d)从图c中用红色框标记的区域放大的区域。[25]
随着使用时间的增加,相邻的阴极粒子将明显地烧结在一起,这减少了电极的总表面积并增加了电池电阻。特别是对于具有NCM阴极的电池,由于Ni2+的原子半径接近Li+的原子半径,随着镍含量的增加,更容易发生Li/TM层间混合。因此,锂离子将更多地卡在阴极离子中,无法参与循环过程。
3)CEI膜的形成及生长
阴极中Li+的损失主要归因于阴极电解质界面(Cathode electrolyte interphase,CEI)膜,其类似于SEI膜[26],但相比于SEI膜,CEI膜具有厚度较薄、成分复合、生长不均匀、状态不稳定、电化学性质特殊的特点[27]。CEI膜由阴极和电解质之间的副反应(如电解质的氧化和LiPF6的降解)产生的化合物组成;过渡金属离子从阴极溶解到电解质中,并由这些金属离子形成的产物也可以作为CEI膜重新沉淀到正极颗粒的表面(图5(a))。此外,有研究揭示SEI分解组分的溶解和迁移可能参与CEI的形成(图5(b))[28, 29]。在高SOC下运行电池将加速电解质的分解,并产生更多的HF来腐蚀阴极,从而产生更多的CEI组分。此外,当电池以高电流率充电和驱动时,副反应也会增加,因为高电流会显著提高温度。电解质在高温下容易分解,这将加速CEI膜的生产。然而,CEI膜对阴极老化的影响不如SEI膜对阳极老化的影响严重。
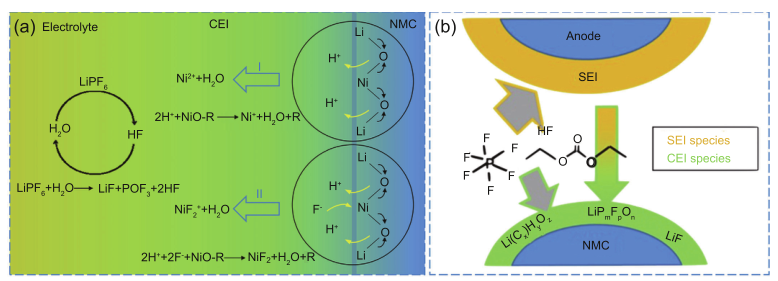
图6 CEI生长机制示意图:(a)表示电解质中锂盐的分解,I和II表示过渡金属在阴极中的溶解及其在阴极表面上的再沉淀。(b)组分迁移形成CEI。[29]
3.电解质的老化机理
电解质决定锂电池的循环稳定性、容量、安全性和操作条件。传统电解质通常由LiPF6和其他有机碳酸盐组成。然而,LiPF6不稳定,容易分解为LiF和PF5,其中PF5与有机碳酸盐反应,导致电解质老化[30]。反应产物在阳极表面上生成SEI膜,在阴极表面上生成CEI膜。虽然稳定且致密的表面膜可以抑制电极表面暴露于电解质,从而有效地减少电解质和电极之间的反应,但在电池循环期间表面膜的连续破裂和再生将继续消耗Li+,这导致电池容量衰退。目前,一些添加剂已添加到电解质中,以形成更稳定的表面膜。此外,在充电状态或高温下,电解液分解并在电池内部形成气体是一种固有的风险,这可能导致严重的事态发展,例如电池内部压力升高、火灾甚至爆炸。
4.隔膜的老化机理
隔膜老化的主要原因通常可追溯到锂枝晶的生长、电解液的腐蚀、隔膜通道的堵塞、高温或高循环次数导致的过度循环和结构退化[31]。特别是,高温(通常在130至150℃的范围内)会导致隔膜软化并关闭其孔隙,从而阻碍电极之间的离子传输,从而导致充放电过程停止。
在商用锂离子电池中,通常使用三层聚丙烯/聚乙烯/聚丙烯(PP/PE/PP)隔膜。PP(熔点165℃)在高温下的变形不是很明显,可以用来确保机械稳定性;PE的功能则是在130℃(PE的熔点)下关闭电池。因此,隔膜(PE/PP/PE)可防止高达130℃的热失控。图7展示了隔膜的关闭行为。阻抗增加与隔膜熔化导致的孔隙结构坍塌有关,两个电极之间形成相对无孔的膜。然而,即使在较低的温度下,聚合物也可能失去孔隙率,从而导致电池在操作期间的阻抗增加[32]。
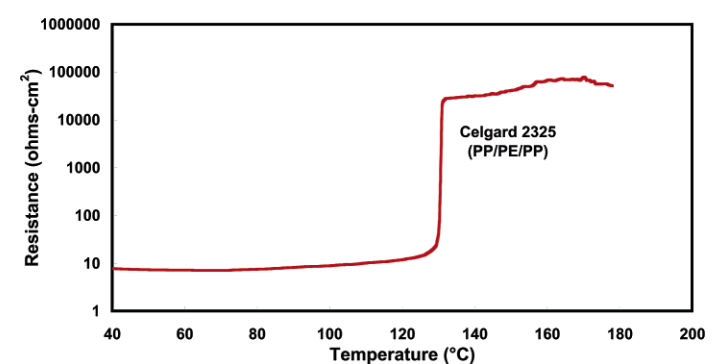
图7隔膜(PE/PP/PE)内部阻抗随温度的变化[34]
此外,过渡金属离子或分解的活性物质的进一步溶解可以通过隔膜扩散并堵塞孔隙[33]。电解质分解产物导致的阻抗增加占电池总阻抗增加的近10%,电解质分解产物会在隔膜上形成一层膜,从而堵塞空穴并阻碍锂离子的传输[33]。
5. 集流体的老化机理
铝箔和铜箔分别是阴极和阳极的集流体使用最广泛的材料。在与阴极充电条件相关的高氧化电位下,铝集电体中发生局部坑状腐蚀[35]。凹坑和腐蚀部位充满金属氧化物产物的混合物,形成结节和表面土丘。铝集流体的性能在很大程度上取决于电解质的组成。由于表面存在氧化铝(Al2O3)和氢氧化铝(Al(OH)3)组成的保护层,金属铝在包含少量氧化剂的有机电解质溶液中通常是稳定的。在LiPF6电解质中,少量的水可以促进电解质的分解并产生稳定的无机盐,从而抑制铝集电体的腐蚀。然而,随着水的产生,电解质的氧化分解产物在铝箔表面发生电化学反应,加速了铝箔的腐蚀。含氟表面面膜的形成对防止有机电解质溶液引起的铝阳极腐蚀具有重要作用。
诸如过放电等极端条件导致铜集流体的电势上升到铜开始氧化为铜离子并溶解在电解质中。在随后的充电过程中,溶解的铜离子沉淀成金属铜并沉积在阳极表面上,导致阳极的锂吸收能力降低和锂电镀的发生。电解液腐蚀导致的锂电镀直接导致容量损失,甚至导致灾难性故障,如内部短路导致的热失控。与铝表面不同,由于阴极保护,铜通常不易在阴极电位下发生局部点蚀。
审核编辑 :李倩
-
锂离子电池
+关注
关注
85文章
3555浏览量
81126 -
铝箔
+关注
关注
0文章
11浏览量
2760
原文标题:锂离子电池老化机理
文章出处:【微信号:电源系统智能管控,微信公众号:电源系统智能管控】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
锂离子电池是如何工作的?了解它的内部结构和制造过程


一文看懂锂离子电池的基础知识

锂离子电池管理:建模、状态估计与故障诊断

一文读懂:锂离子电池的基本结构与应用

锂离子电池的原理与材料全解析

锂离子电池组装:绕线与极耳焊接工艺揭秘

锂离子电池隔膜质量检测与缺陷分析

锂离子电池涂布工艺:技术要求与方法选择

锂离子电池创:性能、分类与GPE的应用前景

锂离子电池化成机理:从分子界面工程到量产工艺的核心解析

锂离子电池电解液浸润机制解析:从孔隙截留到工艺优化

超级电容器与锂离子电池的区别在哪里?




 锂离子电池老化机理
锂离子电池老化机理




评论