生物电信号是人体最基本的生理信号之一,通过对生物电信号的监测可以对多种生理疾病进行诊断和预防。随着微电子科技的不断发展,越来越多的医疗科技选择使用电极贴片与诊断设备集成,以实现实时监测人体健康状况的医疗保健系统,从而对于突发性强、致命性高的心脑血管疾病有着显著的预防作用。
生物电监测电极作为系统硬件的重要组成单元,直接与人体接触采集生物电信号,是生物电传感系统的基础部件。常见的是银-氯化银(Ag/AgCl)凝胶电极,但由于凝胶或粘合剂会对皮肤产生刺激,很难用来长期监测生物电信号。为了实现长效与皮肤接触监测的功能,生物相容性良好的干电极技术近年来得到了一定的发展。然而,由于皮肤的弹性、粗糙质地,附加汗水、油脂、皮屑和毛发等表面特性,干电极技术在皮肤附着力、接触阻抗、透气性等创新优化方面仍面临较大挑战。
由于自然环境下目标附着表面的复杂多样性,依靠单一的黏附机制往往不足以提供生物体稳定的附着和快速运动的能力。几乎所有具有全空间运动能力的生物,均拥有两种及以上的界面附着策略,且生物体型越大,越需要多种附着方式协同作用来提升界面附着力以平衡自重。生物高鲁棒性的附着调控特性依赖于生物脚爪精细的跨尺度附着结构,以及附着结构所呈现的机制之间的协同作用。
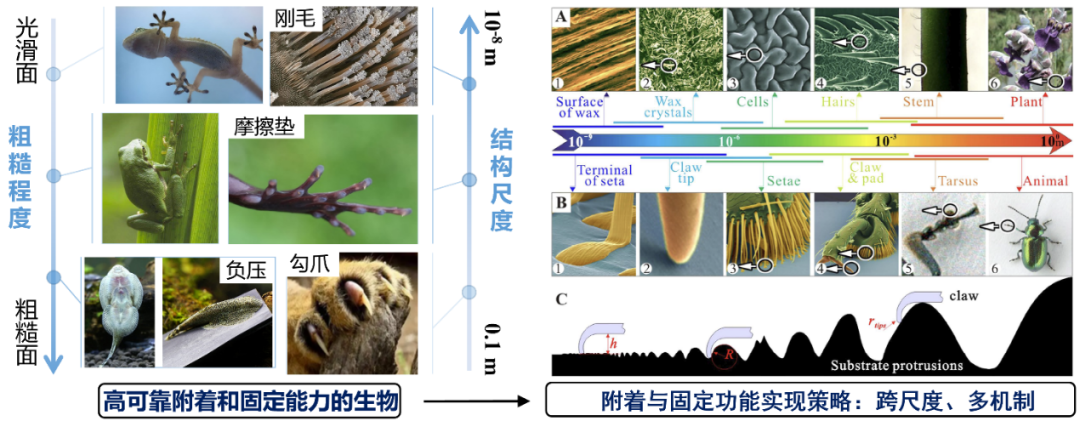
图1 典型具有足端附着能力的生物结构与功能实现策略
基于此,南京航空航天大学姬科举课题组在前期微针摩擦与树蛙湿粘附协同的仿生电极(Advanced materials interfaces, 2022, 2200532)研究基础之上,提出了一种兼具排汗透气性和多机制粘附性能的健康监测电极贴片。相关研究成果以题为“Biomimetic Patch with Wicking-Breathable and Multi-mechanism Adhesion for Bioelectrical Signal Monitoring”发表于期刊ACS Applied Materials & Interfaces。
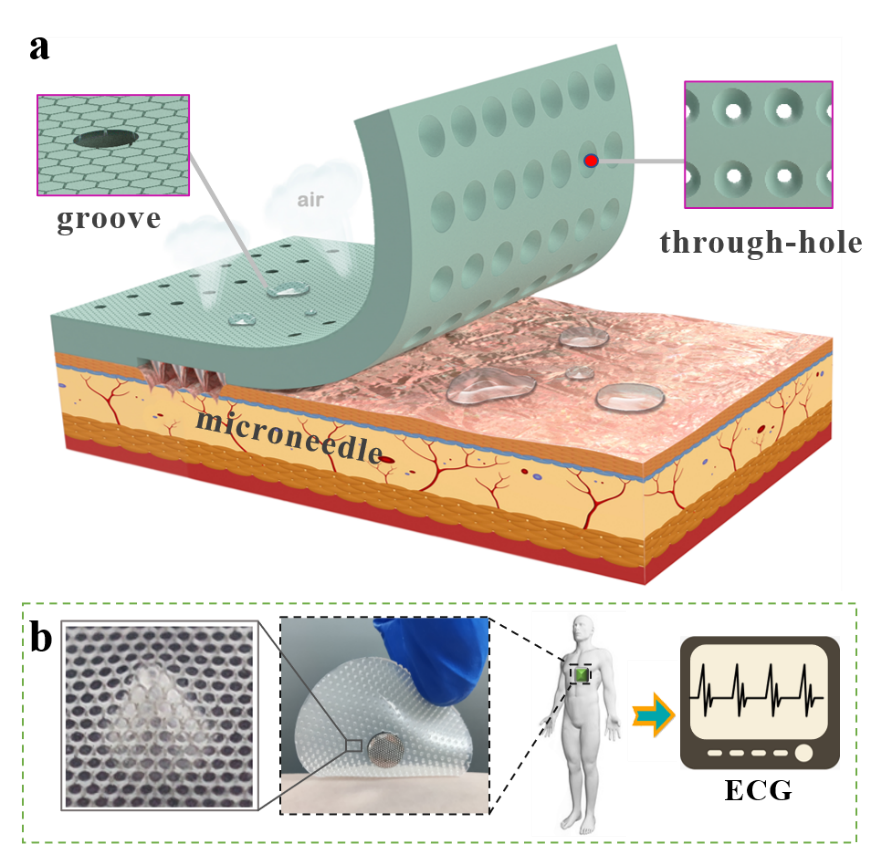
图2 兼具排汗透气性与多机制粘附性能的仿生电极设计
贴片的排汗透气功能采用锥形通孔与蜂窝状微沟槽集成设计来实现,锥形通孔产生的拉普拉斯液相压差和微沟槽的毛细力协同实现了汗液的自驱导流作用;Ag/Ni微针阵列和PDMS-t粘附材料的多机制附着一定程度上保障了电极贴片与皮肤接触的力学稳定性,其中,Ag/Ni微针阵列通过高度控制,形成与皮肤角质层的接触,在保障安全性的前提下,实现了生物电信号采集通道的可靠性。
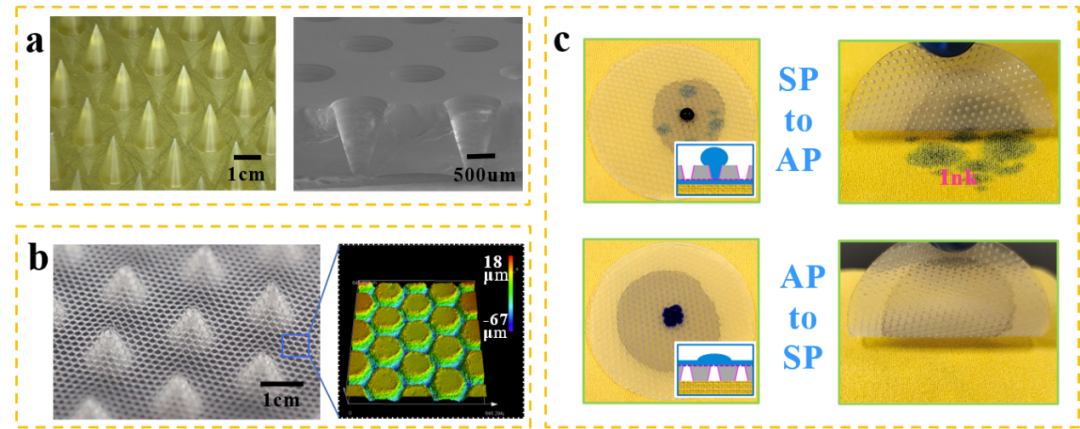
图3 仿生监测电极排汗透气通道结构形貌及其单向自驱导效果图 仿生电极的皮肤界面阻抗测试显示,在100 Hz以下,仿生电极的接触阻抗低于标准Ag/AgCl凝胶电极,在监测志愿者的EMG和ECG生物电信号应用中,仿生电极展示出了较好的静态和动态采集性能。这主要归因于微针阵列与皮肤高阻抗角质层形成机械锁合,与通孔阵列柔性聚合物粘附接触协同作用,增强了仿生电极与皮肤表面的附着力,减少了运动伪影。同时,仿生电极设计中汗液的自驱导流结构保障了皮肤排汗透气的需求,具有良好的皮肤接触生物相容性,为实现长效的健康监测提供了新思路和新途径。
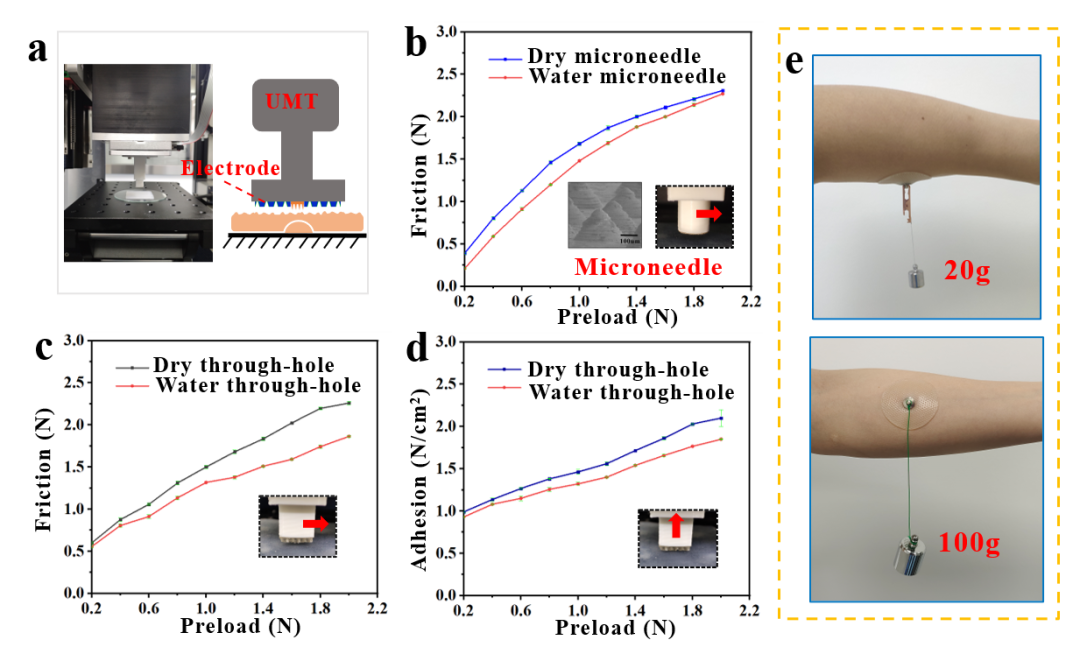
图4 仿生电极贴片切向摩擦力和法向粘附力量化测试实验
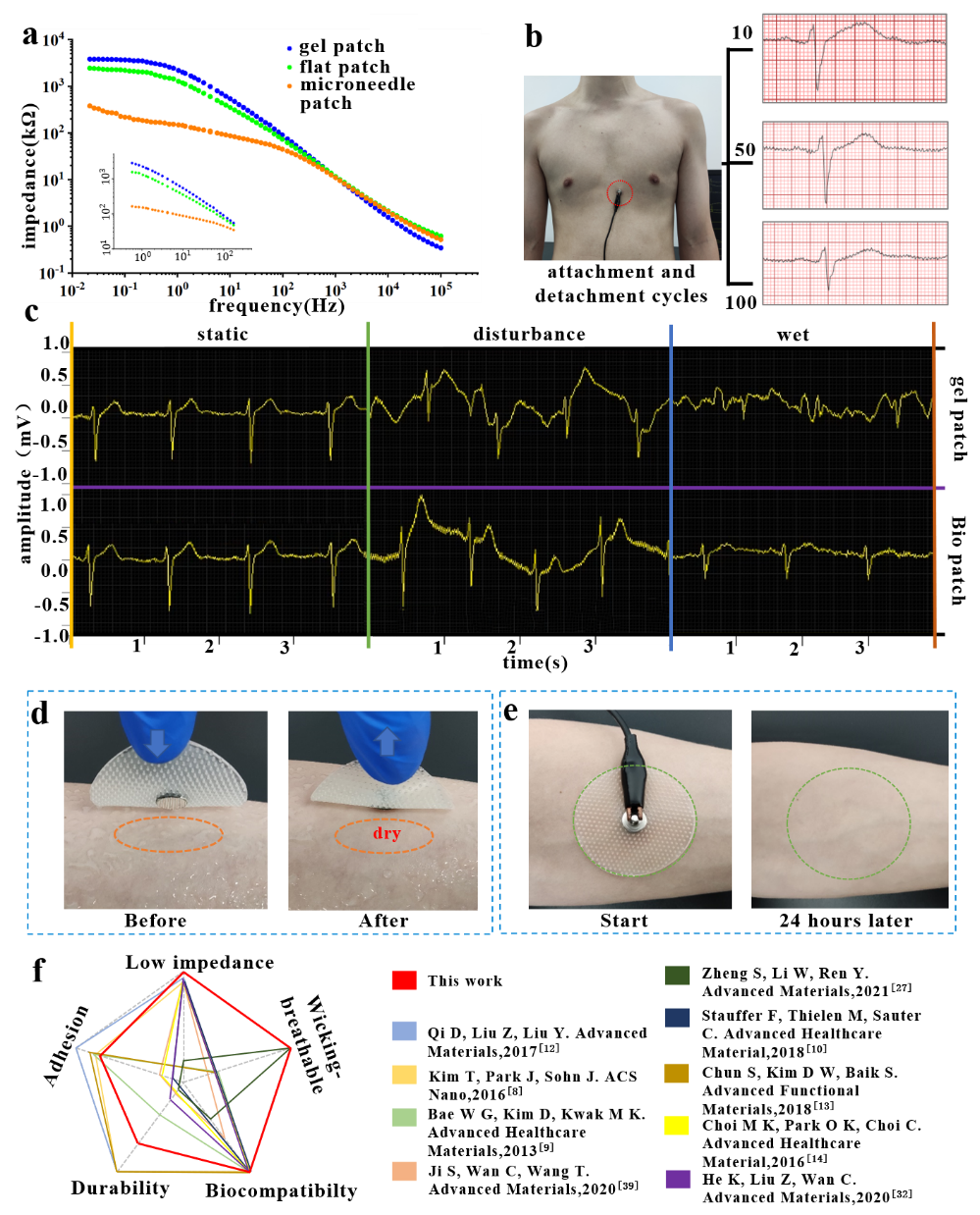
图5 仿生电极贴片心电监测性能及其与皮肤接触的生物相容性评价 论文第一作者为南京航空航天大学机电学院硕士研究生张迁,论文通讯作者为姬科举副研究员,南京航空航天大学为第一完成单位。本研究工作得到了国家自然科学基金、南京市医学科技发展基金、江苏省仿生功能材料重点实验室基金等项目的资助。
论文链接: https://pubs.acs.org/doi/full/10.1021/acsami.2c13984
审核编辑 :李倩
-
电极
+关注
关注
5文章
813浏览量
27215 -
生物电信号
+关注
关注
0文章
5浏览量
9643
原文标题:兼具排汗透气性和多机制粘附性能的仿生贴片,用于生物电信号监测
文章出处:【微信号:Micro-Fluidics,微信公众号:微流控】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
DFT在生物信号分析中的应用
低电平灵敏专用仪器的技术原理和应用场景
CBM24AD99Q | 重塑生物电势测量,开启精准医疗新时代

芯佰微电子CBM24AD99Q模数转换器(ADC) 助力生物电势测量技术





 生物电信号的监测可以对多种生理疾病进行诊断和预防
生物电信号的监测可以对多种生理疾病进行诊断和预防










评论