【研究背景】
界面性质决定了电化学系统的各种功能。锂金属负极提供最高的理论比容量和最低的电化学势,但锂金属和液体电解质之间的界面不相容性会导致剧烈的副反应,使得活性锂持续转化为“死锂”金属和固体电解质界面相(SEI),造成锂金属电池的快速容量衰减。因此探索这些非活性锂物种的组成、功能和形成机制对于理解锂金属电池的失效机制至关重要。但是研究具有复杂成分的SEI对目前大多数分析技术都是极具挑战的。目前人们普遍认为SEI组分可分为两部分:有机组分:ROLi、RCOCO2Li等和无机组分:Li2O、LiOH、Li2CO3、LiF等,并且这些SEI物种都被认为是由固态锂金属和液态电解质之间的(电)化学反应形成的。然而需要注意的是,电池系统中的化学物质不限于液态电解质和固态电极。锂离子电池中也广泛报道了氢气、乙烯、二氧化碳等气体种类。尽管许多气体会自发地与锂金属发生反应,如二氧化碳和氧气,但气体物质与锂金属之间的反应在电池化学中很少被讨论。
最近,一些研究表明锂金属会与氢气反应,在锂金属电池中生成氢化锂(LiH)。Aurbach等人首先讨论了锂金属在室温下与H2反应形成LiH的可能性。Kourkoutis等人发现,LiH的量比电解液中微量水可产生的H2大一个数量级,认为有机溶剂的还原也可能促进H2的形成。然而Lucht等人证明,有机溶剂的化学还原不会产生H2,但会产生碳氢化合物,如乙烯、丙烯和乙烷等。因此,LiH与循环过程中形成的H2之间的直接相关性尚不完全清楚。此外,一个问题仍然存在:是否有其他气体可以与锂金属反应,导致未发现的非活性锂物种?
【工作简介】
近日,厦门大学杨勇教授课题组等人首先应用电化学原位质谱法(OMS)将LiH的演化与气体形成相关联,证明乙烯是整个循环过程中主要的连续形成的气体物种。使用质谱滴定(MST)技术结合13C和2H同位素示踪法,证明了乙烯和锂金属可以反应生成LiH和碳化锂(Li2C2)。这是一个尚未揭示的LiH形成机理,也是Li2C2形成机制的首次报告。并且利用相场模拟,证实了气泡的存在会改变界面处的电场和离子浓度分布,从而导致不均匀的锂金属沉积和死锂形成。通过合理设计电解质,证明了抑制乙烯的形成可以进一步抑制LiH和Li2C2的形成,并在石墨负极中验证了这一结论的适用性。相关成果以“Gas induced formation of inactive Li in rechargeable lithium metal batteries”为题发表在国际顶级期刊Nature Communications上。向宇轩博士(厦门大学2021届博士,现任西湖大学青年研究员)、厦门大学博士生陶明明和陈晓轩为本文共同第一作者。通讯联系人为厦门大学杨勇教授
【内容详情】
1. 关联LiH的形成与气体演化
作者利用质谱滴定(MST)技术作为定量方法,研究了使用1M LiPF6/EC:EMC(基础电解液)的LiFePO4||Cu电池中形成的LiH的演变。重水(D2O)作为滴定剂和非活性锂反应形成各种气体。其中,HD气体仅由LiH根据以下反应生成:LiH+D2O=LiOD+HD↑。HD信号在质谱中呈现出独特的质荷比(m/z=3),因此可用于跟踪LiH的演变(图1a)。同时,D2O与死锂金属反应生成D2(m/z=4),其演变代表死锂金属的形成。图1b显示,HD和D2信号的积分面积都随着循环次数的增长而不断增加,显示出它们的不可逆累积,这会导致活性锂的持续损失。为了将LiH的形成与H2气体相关联,作者采用电化学原位质谱技术(OMS)监测电池中产生的各种气体,包括H2(m/z=2)、乙烯(C2H4)(m/z=28)、乙烷(C2H6)(m/z=30)和CO2(m/z=44)。值得注意的是,H2的形成主要在第一次充电过程中观察到,但在长时间循环中没有检测到(图1c)。这种现象与之前报道的硅负极和Cu||NCM111电池中的观察结果一致,其中H2的形成被认为来自电解液中痕量水的分解。因此仅在初始循环中占主导地位。基于LiH是由锂金属和H2之间的反应产生的假设,H2的这种演化模式不能合理解释MST结果中观察到的整个循环过程中LiH的持续形成,这表明在长时间循环中LiH还有其他未揭示的形成机制。
与H2相反,作者观察到了C2H4在整个循环过程中持续形成(图1c)。对于每一个循环,C2H4信号在充电期间开始上升,并在放电时突然衰减,这表明C2H4的形成伴随着锂沉积。已经有研究充分表明,C2H4是EC溶剂通过双电子还原反应的分解产物:EC+2e-à (CH2OCO2Li)2+C2H4。除了OMS观察到的C2H4外,滴定的CO2(由D2O与(CH2OCO2Li)2之间的反应产生的)结果也表明(CH2OCO2Li)2持续增加。OMS和MST结果表明了LiH形成和电解质分解是同时进行的。考虑到有机电解液是电池中质子的主要来源,这一并发过程暗示了LiH的形成和C2H4演化之间的潜在关联。
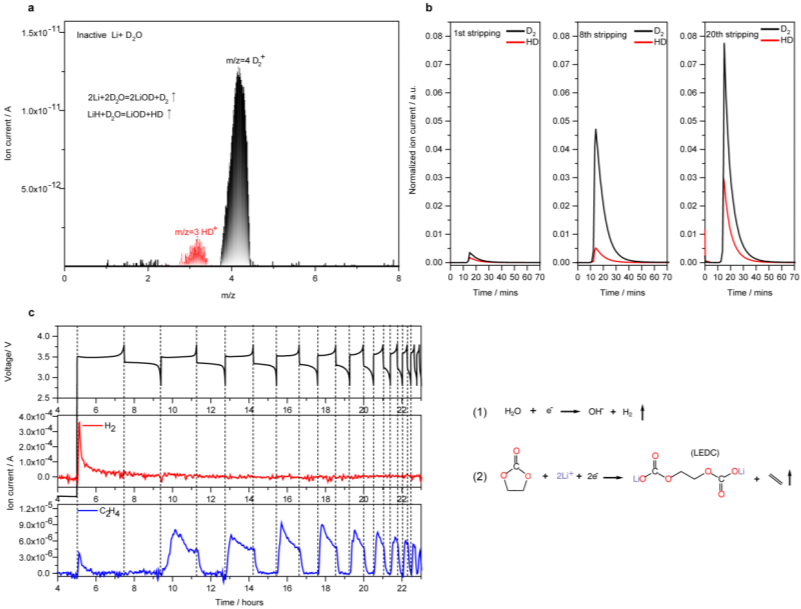
图1 使用1 M LiPF6/EC:EMC电解液的Cu||LiFePO4电池中LiH以及气体物种的演变。a非活性锂与D2O反应产生的气体产物的质谱。b基于反应2Li+2D2O=2LiOD+D2↑和LiH+D2O=LiOD+HD↑ 的死锂金属和LiH质谱滴定结果。c Cu||LiFePO4电池在2.8 V至3.8 V之间以0.75 mA cm-2循环的电压曲线,以及H2(m/z=2)和C2H4(m/z=28)的相应电化学原位质谱结果。
2. 锂金属与乙烯的反应
Guntz等人于1896年首次报道了锂金属与乙烯的反应。C2H4在加热气氛下与锂金属反应生成灰白色产物,其化学成分为LiH和Li2C2的混合物:
C2H4+6Li0→4LiH+Li2C2 (式1)
然而,在电池化学中,这一反应是否能在室温下进行尚不清楚。作者首先计算了该反应的吉布斯自由能(298.15 K)为-398.049 kJ/mol,表明该反应在室温下热力学可行。作为参考,锂金属与H2反应生成LiH的吉布斯自由能为-136.894 kJ/mol。为了直接证明该反应的在室温下的可行性,作者将纯锂金属箔在C2H4(99.999%)和氩气(99.999%)气氛中分别储存10天,然后刮去表面物种并通过MST技术进行分析。基于反应:Li2C2+2H2O à 2LiOH+C2H2可以通过乙炔(C2H2)的信号(m/z=26)验证Li2C2的存在。使用H2O而不是D2O作为滴定剂,可以避免CO2碎片(CO+,m/z=28)对m/z=28(C2D2)的分析的干扰。滴定结果表明,两个样品的反应气体均以H2为主,但重要的是,仅在C2H4储存的锂金属样品中观察到C2H2信号,证明锂金属和乙烯反应产生了Li2C2。
尽管已经证明了式1的可行性,但Li2C2在非活性锂中的存在仍然是不明确的。Schmitz等人首先通过观察乙炔阴离子的拉曼信号,提供了锂金属表面形成Li2C2的光谱证据。然而,问题仍然存在:Li2C2在循环过程中是如何演变的?Li2C2的演变是否与LiH具有相同的趋势?在此,作者采用MST技术研究了Cu||LiFePO4电池中形成的非活性锂中Li2C2的存在和演变。图2a显示了在20次循环后,使用H2O滴定剂对基础电解液中形成的非活性锂的典型滴定结果。信号C2H2(m/z=26)的存在验证了Li2C2的存在,证明了其不可逆性质,这在锂金属电池中尚未讨论。作者对第1、第8和第20次循环后形成的非活性锂进行了MST测试,发现Li2C2(图2b)与LiH(图2c)具有相似的演化模式。这两种非活性锂物种的相互形成和增加也证实了式1的可行性。
为了进一步证明LiH和Li2C2的形成与乙烯(EC分解的产物)直接相关,作者使用了三种同位素标记的EC:全氘代EC(D4-EC)、羰基碳标记的EC(13C1-EC)和全碳标记的EC(13C3-EC),以取代天然丰度的EC(未标记的EC),形成LiPF6/EC:EMC电解液。使用H2O作为滴定剂滴定D4电解液和未标记电解液中形成的非活性锂,仅在D4电解液中观察到DH+(m/z=3)信号,证实了LiD的形成。该结果证实了LiH的形成与EC溶剂中的质子直接相关。此外,当使用D2O滴定13C1电解液和13C3电解液中形成的非活性锂时,主要在13C3电解液中观察到13C2D2+(m/z=30)信号,而13C1电解液与未标记电解液的信号较小。这表明Li2C2的形成主要与非羰基碳有关,非羰基碳也是C2H4的来源(图1中反应2)。
此外,作者检查了所有报告Li2C2存在的文献,发现无论电解质配方如何变化,这些报告中都使用了EC溶剂。此外,低温电子显微镜(cryo-EM)结果显示乙烯气泡和LiH都存在于锂金属界面。这种空间接近性也为锂金属和乙烯的反应提供了可能性。值得注意的是,不能完全排除其他溶剂会产生乙烯的可能性。因此,在未来的类似研究中,应谨慎使用能够生产乙烯的其他溶剂或添加剂,因为这可能会导致额外形成LiH和Li2C2。LiH和Li2C2的其他形成机制可以在未来的研究中探索。正如氟化锂(LiF)在电池化学中有不同的形成途径一样,这在很大程度上取决于使用的溶剂和添加剂。
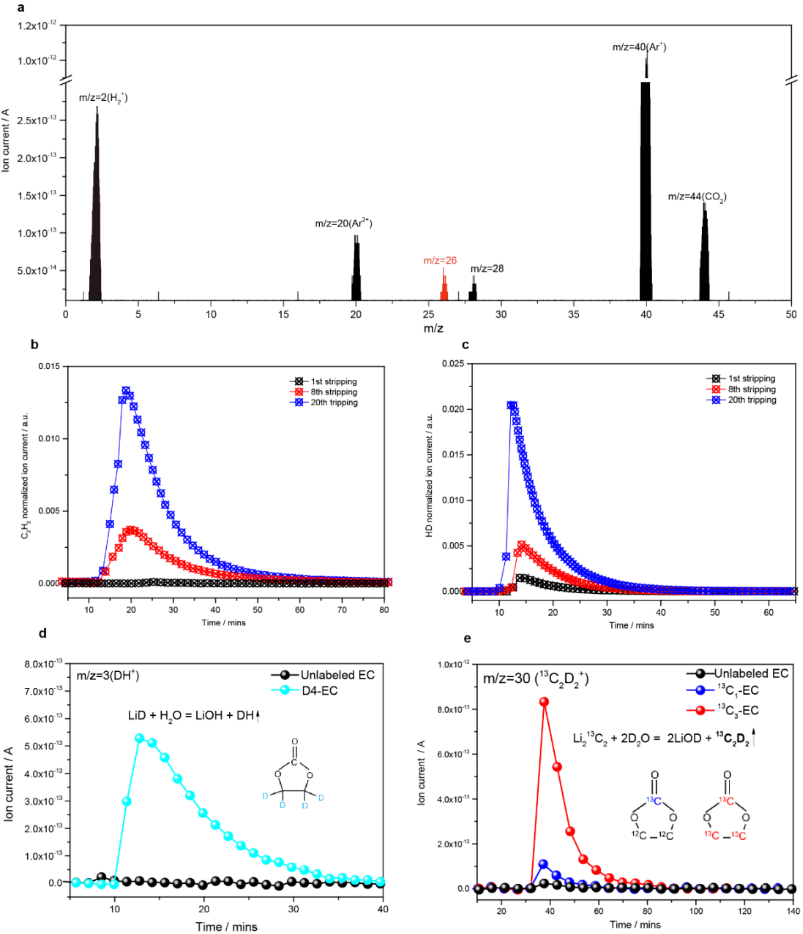
图2 锂金属与乙烯之间的自发反应。a使用H2O的非活性锂的质谱滴定结果。信号C2H2(m/z=26)表示Li2C2的形成。b C2H2(m/z=26)信号和c HD(m/z=3)信号的演变,分别代表Li2C2和LiH的积累过程。d未标记EC和全氘代EC(D4-EC)中形成的非活性锂的质谱滴定结果。e未标记的EC、羰基碳标记的EC(13C1-EC)和全碳标记EC(13C3-EC)中形成的非活性锂的质谱滴定结果。
3. 气体对锂沉积的影响
作者比较了常见无机SEI物种中锂扩散的能量势垒和带隙。锂离子在Li2C2中的扩散比Li2O和Li2CO3慢得多,但与离子电导率极小的LiF相当。并且LiH和Li2C2的带隙低于Li2O、Li2CO3和LiF的带隙,这表明其具有潜在的较高电导率,这对电池性能不利。因此,考虑到离子电导率和电子电导率,LiH和Li2C2被认为是在锂金属表面上形成的非理想SEI物种,可能导致较大的界面阻抗和不均匀的锂离子通量。
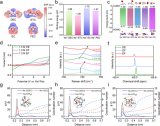
除化学效应外,气体对电化学过程的机械效应在析气电极中被广泛研究,如水分解和CO2电还原。在这些系统中,气泡会减少电化学活性面积并阻断离子传输路径,但锂电池中很少讨论气泡对锂沉积的影响。作者首先使用COMSOL模拟来探索气泡对Li+浓度和电场分布的影响。首先对附着在集流体上的非Li+和非电子导电气泡进行建模。模拟结果表明,气泡将导致Li+浓度(图3a)和电场(图3b)的不均匀分布,这被认为是锂枝晶生长的原因。然后作者进一步采用相场模型来描述沉积的锂金属的形态。没有气泡效应,Li+和电场的均匀分布将导致沉积的锂金属同时水平和垂直生长,呈现苔藓型形态(图3c),如光学显微镜所观察到的。当气泡附着在铜箔上,沉积金属的水平生长受到极大抑制(图3d)。在这种情况下,沉积的锂金属倾向于形成枝晶。在气泡漂浮在铜箔上的情况下观察到了相同的情况(图3e)。图3f总结了沉积的锂金属的长度和宽度,表明非Li+导通气泡的存在和及其空间分布将促进锂枝晶的形成。有趣的是,我们观察到沉积的锂金属会在气泡表面生长。在这种情况下,气泡的分离(detachment)会使一些锂金属碎片从本体上悬垂,形成死锂金属。这些结果表明,死锂金属不仅可能在剥离过程中形成,气体分离也会导致死锂金属的形成。
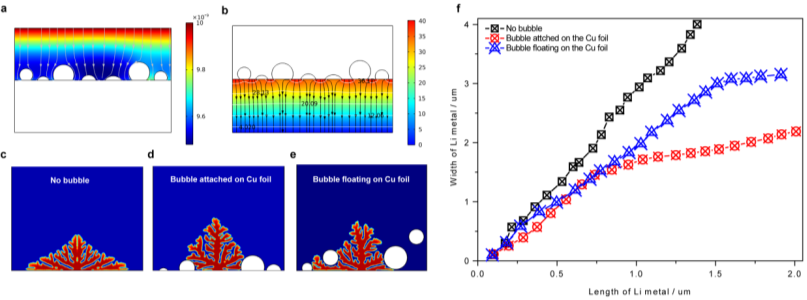
图3 气体对锂金属沉积的影响。铜表面附着有气泡的a Li+浓度和b电场分布的模拟。通过相场模拟探讨了气泡对沉积锂金属形态演变的影响:c无气泡,d有气泡附着在铜表面,e漂浮在铜箔上。f气泡对枝晶长度和宽度的影响。
4. 抑制LiH和Li2C2的形成
上述结果表明,LiH和Li2C2的形成与乙烯的演化高度相关,因此通过仔细选择电解液配方来抑制乙烯的形成是防止Li2C2和LiH进一步形成的关键。作者首先去除基础电解液中的EC溶剂以形成1 M LiPF6/EMC(EMC电解液)。尽管在EMC电解液的非活性锂中未检测到Li2C2,但具有这种无EC电解质的电池在第一次循环后损失了几乎99%的容量(图4a)。Li2C2的形成减少也可能来自有限的循环寿命,使得无法得出可靠的结论。因此,保持溶剂(EC:EMC)不变,用LiODFB取代基础电解液中的LiPF6,形成1 M LiODFB/EC:EMC。LiODFB在锂金属上优先分解形成所谓的阴离子衍生SEI并防止溶剂的进一步分解。图4a显示了具有LiODFB电解液电池的优异循环性能,证明了LiODFB的保护作用。原位质谱结果表明,H2的形成在最初的三个循环中占主导地位,然后随着循环的延长而衰减。在相同的循环时间(20小时)下,分别对LiODFB和基础电解液的H2面积进行积分也显示出可比较的值,表明两种不同电解液产生的H2量相似。并且在整个循环过程中使用LiODFB电解液时未检测到C2H4的形成,表明EC的分解得到了很好的控制。基于上述结果和式1,我们可以得出结论,使用LiODFB大大抑制了EC分解。
为了验证上述假设,作者进行MST测试研究LiODFB电解液中LiH和Li2C2的演变。图4显示,当使用LiODFB电解液时,Li2C2和LiH的信号都受到抑制。LiH仍然存在于LiODFB电解液中,但与基础电解液中的持续增加不同,LiH的形成主要来自第一个循环,并且在延长的循环中缓慢增加。这一结果与LiODFB电解液中的气体演化一致:H2在初始循环中占主导地位,而C2H4在整个循环过程中受到抑制。
此外,作者用醚基溶剂完全取代碳酸酯溶剂:1 M LiTFSI/DOL:DME+2wt% LiNO3。醚基电解液与锂金属的结合更加稳定,电解液分解较少,并且MST结果也表明了LiH和Li2C2的相互抑制。此外,作者模拟了石墨||LiFePO4电池中的析锂,在20次循环后,回收石墨负极并用D2O和H2O滴定。在石墨负极中也观察到类似的情况:在LiODFB电解液中,与基础电解液相比,LiH和Li2C2都受到抑制。
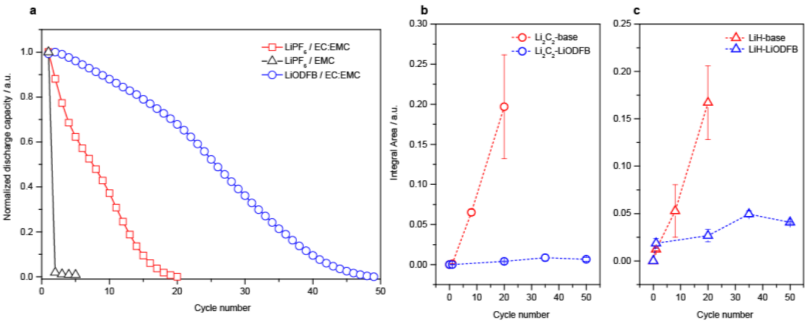
图4 通过电解质优化抑制LiH和Li2C2。a Cu||LiFePO4电池的循环性能,使用1 M LiPF6/EMC、1 M LiPF6/EC:EMC(基础)和1 M LiODFB/EC:EMC(LiODFB)电解液在2.8 V和3.8 V之间循环,固定电流密度为0.75 mA cm-2。基础电解液和LiODFB电解液中形成的非活性锂的b Li2C2和c LiH的相应滴定结果。误差条来自三次独立实验。
5. 气体诱导的非活性锂形成
经典SEI模型侧重于固液两相界面。因此,非活性锂的形成通常被认为源于两个过程:(1)固相过程,即死锂金属的形成过程仅涉及固体(锂金属);(2)液相过程,其描述了锂金属与液体电解质之间反应形成SEI(图5a)。然而,第三个过程:气体参与的非活性锂形成很少被讨论。
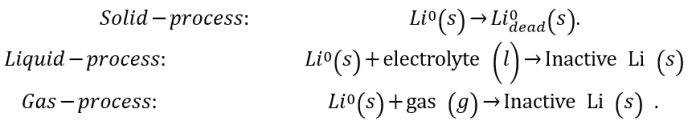
作者揭示并强调了锂金属和气体物种之间的化学反应(在图5a中表示为气相过程)。以乙烯气体为例,1 mol乙烯可以与6 mol锂金属反应生成非活性锂,而1 mol EC的分解仅产生0.5 mol非活性锂(LEDC)。这强调了气体对非活性锂形成的显著影响。基于质谱的定量能力,作者区分并量化了通过这三个过程形成的非活性锂。死锂金属、LiH和Li2C2分别通过D2、HD和C2H2的滴定信号定量。这里假设Li2C2和LiH完全由锂金属和气体物种之间的化学反应形成,其余的非活性锂由液相过程形成。液相过程中形成的非活性锂的量可以通过以下方程式计算:总的不可逆锂-(死锂金属)-LiH- Li2C2。图5b显示了使用基础电解液的Cu||LiFePO4电池中形成的非活性锂的定量结果。LiH和Li2C2对非活性锂形成的贡献是20次循环后容量损失的19.0%。相比之下,该值在LiODFB电解液中仅为3.2%。在LiODFB电解液中更好的电池循环性能可归因于在整个循环过程中形成的LiH和Li2C2较少,这突出了抑制气体析出以实现锂金属电池更长循环寿命的重要性。
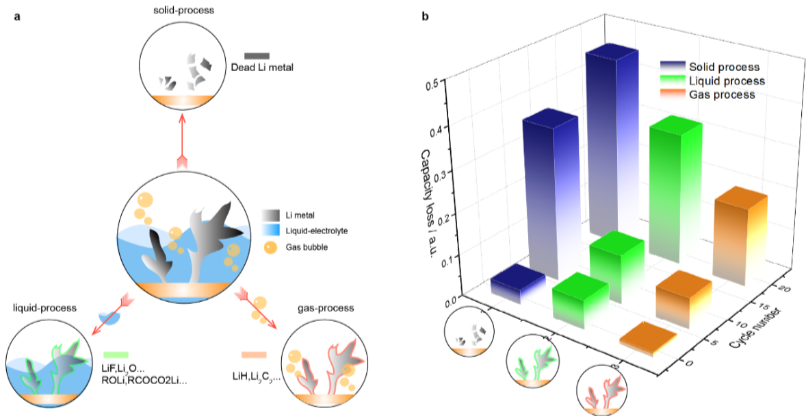
图5 通过质谱滴定法确定的非活性锂的三种形成过程及其相应的量。a通过(i)固相过程形成非活性锂的示意图:形成死锂金属;(ii)液相过程:通过液体电解质与锂金属之间的反应形成非活性锂;(iii)气相过程:通过气体物种与锂金属之间的反应形成非活性锂。b基础电解液中的非活性锂分布。假设Li2C2和LiH都是由锂金属和气体物种之间的化学反应形成的。其余的非活性锂(排除死锂金属、LiH和Li2C2)由锂金属和液体电解质之间的反应形成。
【总结与展望】
在本文中,作者首次揭示了乙烯(EC分解的副产物)与LiH具有类似的积累模式。利用MST和同位素示踪方法,系统地研究了锂金属与乙烯之间的反应,该反应将促进非活性锂(Li2C2和LiH)的形成。相场模拟结果表明,气泡的存在会影响沉积锂金属的形态,并导致更多的枝晶形成。通过合理选择电解质配方,能够抑制乙烯的形成,并进一步抑制锂金属和石墨负极中LiH和Li2C2的形成。本文的结果强调了一种被忽视的非活性锂形成途径,即气体诱导的惰性锂,这在电池研究中很少被讨论,也缺乏全面的研究。
审核编辑 :李倩
-
电解质
+关注
关注
6文章
821浏览量
20264 -
光谱
+关注
关注
4文章
853浏览量
35506 -
锂金属电池
+关注
关注
0文章
140浏览量
4419
原文标题:厦门大学杨勇教授课题组Nature Communications:可充锂金属电池中气体诱导的非活性锂形成机制
文章出处:【微信号:Recycle-Li-Battery,微信公众号:锂电联盟会长】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
全固态锂金属电池的最新研究
筛选理想的预锂化正极应用于无负极金属锂电池

高能锂金属电池中的宏观均匀界面层与锂离子传导通道
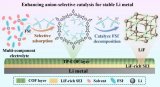
通过电荷分离型共价有机框架实现对锂金属电池固态电解质界面的精准调控




 可充锂金属电池中气体诱导的非活性锂形成机制
可充锂金属电池中气体诱导的非活性锂形成机制
















评论