口服蛋白质类药物容易在胃肠道中降解,造成吸收效果减弱,而且还要在肠道菌群中维持稳定,穿过粘液屏障,才能发挥生物药效。例如胰岛素口服的生物利用率不足1%,对于数以百万计的糖尿病患者来说,每天打针是一件很麻烦且痛苦的事情。如何突破粘液屏障,让大分子药物最大程度地发挥药性,使广大病患免遭注射之苦?
来自美国麻省理工学院的Robert Langer、GiovanniTraverso团队开发了一种可口服的药物输送胶囊,在微型马达作用下旋转前进,局部清除粘液屏障,并在肠液的pH激发下释放药物。该工作以“RoboCap: Roboticmucus-clearing capsule for enhanced drug delivery in the gastrointestinal tract”为题,发表在Science Robotics期刊上。
Robocap机器人胶囊尺寸与“000”号胶囊一致,在RoboCap内部,横向安装在电机上的偏置配重产生向心力,使RoboCap克服表面摩擦振动和旋转。表面覆有凝胶状物质防止吞咽时造成不适,胃液的腐蚀会使Robocap露出表面结构,到达小肠后,肠液的pH触发胶囊内的马达开始旋转工作(图1A),与小肠皱襞、绒毛、粘液相互作用提高药物输送(图1E-1H),随着每一次旋转,药物负载一层层地剥落,沉积药物颗粒。RoboCap活动约35分钟,通过蠕动沿着肠道移动,最终通过排便清除。
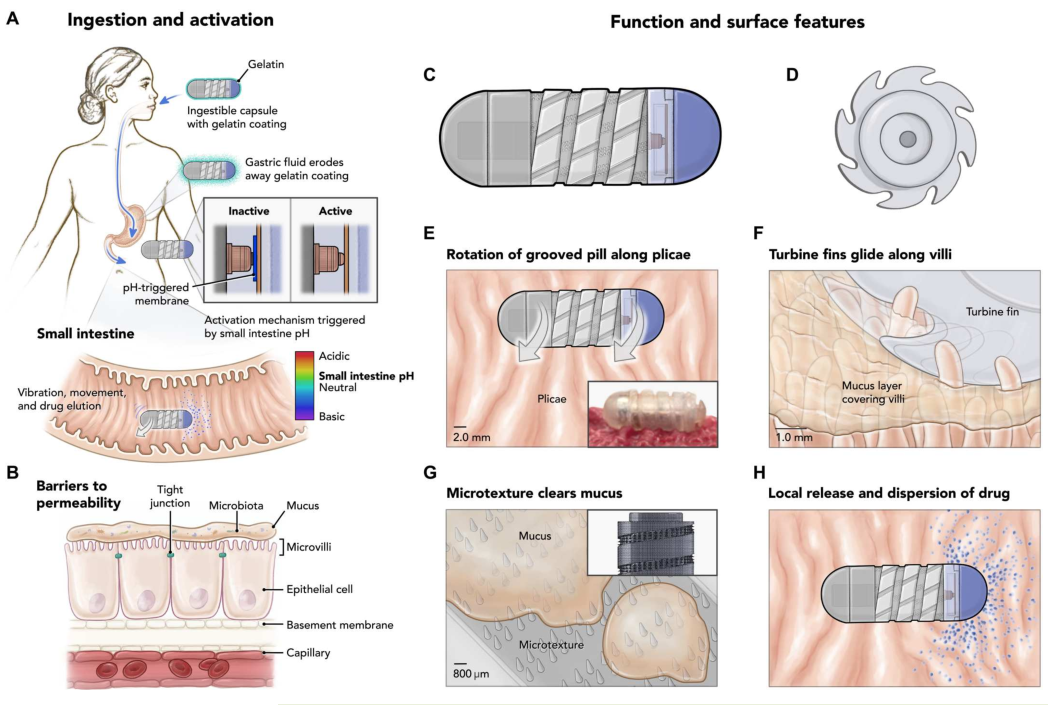
图1 Robocap进入胃肠道并与小肠表面相互作用
为了优化旋转情况以更好地清除粘液,研究人员对比了几种几何外形,其中螺旋凹槽型速率明显提升(图2C、2D)。在水、空气、食糜、粘液介质下测定了其旋转速率,粘度越高旋转速率越慢,但该速率差异不超过30%(图2E)。当RoboCap贴近小肠内表面时,在螺旋形外壳的凹陷处分布着螺钉(图1G)来阻断粘液层,高度为800 μm的螺钉表现最好的吸液和清除粘液的能力(图2G、2H)。受鱼雷叶片的启发,研究人员在螺旋形外壳中加入了作为涡轮叶片的圆形狭缝,以将排出的粘液推进管腔,并增强管腔流体的混合。
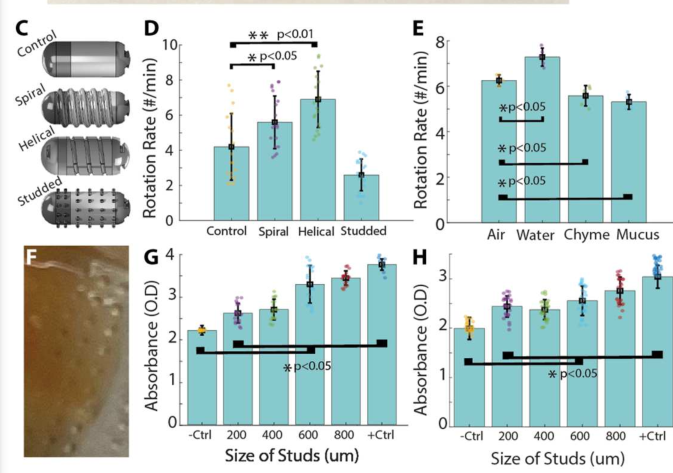
图2 不同几何外形的胶囊清除粘液效果
对不同运动频率下的反应室进行成像,腔室中对液体样品进行吸光度测量表明,与对照相比,RoboCap能够更快地溶解药物,并具有更大的空间分散性(图3I)。借助Franz扩散池进行了万古霉素的体外扩散实验,无论是平滑或是螺旋凹槽型的Robocap,药物渗透量都显著增加了10倍(图3A、3B)。随后进行了耐化学性测试,激活机制关闭的RoboCaps浸入37°C的模拟胃液或肠液中72小时,移除后,100%的胶囊能够被激活并正常工作。
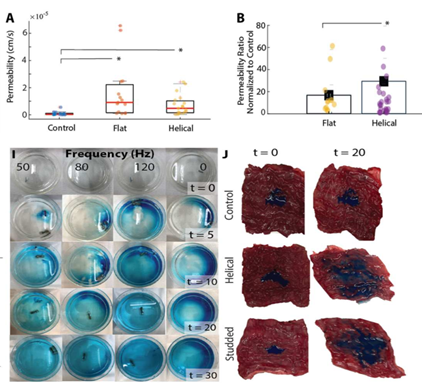
图3Robocap的药物扩散能力
研究人员将负载万古霉素的Robocap应用于麻醉猪中,同体外实验一样,螺旋凹槽型渗透性显著提高(图4C、4D)。对比内窥镜腔内喷雾与Robocap输送胰岛素,Robocap的采用使血糖浓度显著降低,血液中胰岛素含量上升(图4E、4F),观察到的组织渗透性比先前报道的大两倍以上,甚至有3只动物在60 min时出现了低血糖症状。
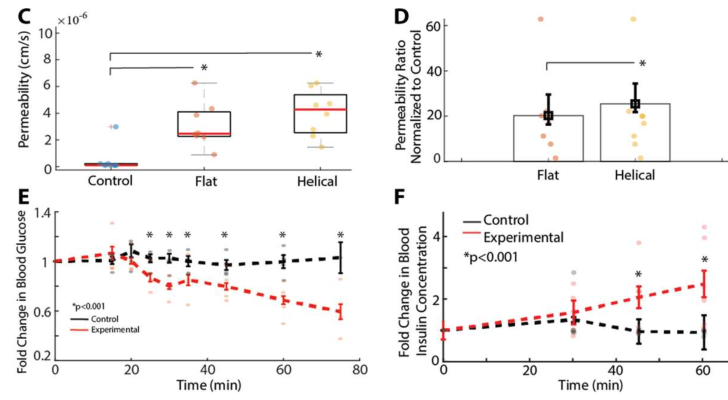
图4Robocap在猪体内的万古霉素和胰岛素输送实验
为了观察药物在组织中的渗透,研究人员在RoboCap中封装了一种蓝色染料,并在体外施用于小肠组织。与口服给药对照组(图5J)相比,可以看到蓝色颗粒更深入地渗透到用RoboCaps处理的微绒毛和上皮层中(图5K、5L)。口服或内窥镜输送到小肠后,RoboCaps安全地通过动物的胃肠道,无穿孔或梗阻。通过RoboCap活动前后进行的内窥镜检查(图5H、5I),也没有发现粘膜糜烂、炎症感染或血液学并发症。
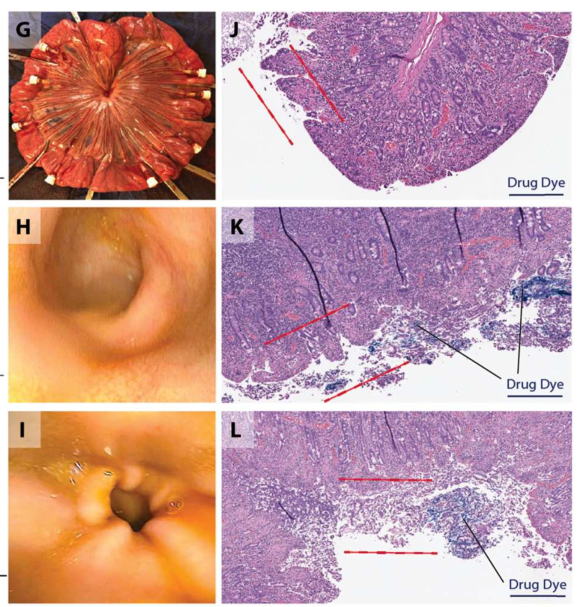
图5Robocap的组织渗透情况及安全性检验
Robocap作为一种可口服的药物输送胶囊,受到胃肠道液pH的触发暴露出表面结构,通过旋转运动可局部清除粘液层,增强管腔混合,并将药物负载局部沉积在小肠中,以增强药物吸收。胶囊设计可以进一步增强,例如,胶囊采用两头相对旋转机制可以增加周围流体的混合;修改可溶膜实现pH敏感性调整,以瞄准胃肠道的其他部位。RoboCap可以装载特定药物实现个性化给药,还可以帮助美沙拉嗪和皮质类固醇等药物的局部给药治疗。
审核编辑:刘清
-
机器人
+关注
关注
211文章
28418浏览量
207070
原文标题:可口服的粘液清除型“机器人胶囊”,用于胃肠道中药物输送
文章出处:【微信号:Micro-Fluidics,微信公众号:微流控】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐




 可口服的粘液清除型机器人胶囊可用于胃肠道中药物输送
可口服的粘液清除型机器人胶囊可用于胃肠道中药物输送












评论