研究背景
过去数十年的商业化,锂离子电池(LIBs)取得了长足发展,已然接近其理论能量密度的极限,促进了锂金属化学的复兴。然而,锂金属电池遭受着脆弱的固体电解质间相(SEI)和低的脱溶剂化动力学的阻碍。因此,迫切需要优化电解质溶液以调控电池的SEI化学和界面处的脱溶剂动力学,从而匹配电池系统的运行。电解质工程是电池研究的热点领域之一,其中溶剂化作用与电池界面化学高度相关。大量研究表明,阴离子引入的Li+溶剂化结构,如高浓度电解质(HCEs),局部高浓度电解质(LHCEs),和弱溶剂化电解质(WSEs),可以促进富含无机物的SEI/正极电解质间相(CEI)生成,以此稳定电极/电极界面而有效提升电池的长循环寿命。到目前为止,电解液的研究主要集中于采用什么方式或策略调控阴离子溶剂化结构的构建,很少有人关注锂离子与溶剂间的络合方式这一本质基础,其对溶剂化壳层具有重要影响。
成果简介
近期,清华大学李宝华教授和昆明理工大学特聘教授王贤树通过Li+和单溶剂分子[双(2-甲氧基乙氧基)甲烷,缩写为“BME”]之间特殊的双/三络合作用实现对锂离子溶剂化结构的调控作用。利用BME分子中的多氧位络合位点形成的溶剂化特征,其不同于传统的1,2-二甲氧基乙烷(DME)分子体系。在1.0 M的常规浓度下,单盐、单溶剂电解液体系(LiFSI-BME)包含了富阴离子型溶剂化鞘,促进了富含无机物的SEI形成,从而提升离子迁移动力学,可逆的锂沉积/溶解,以及宽温条件下的无枝晶形貌。因此,锂金属电池表现出良好的倍率性能和超长的循环寿命,甚至是在高负载正极,有限锂源,高低温和高容量软包电池的苛刻条件下,其电化学性能也能够显著改善。我们的研究工作提出一个电解质设计的新原则,强调溶剂分子对溶剂化结构优化作用,这对于锂金属电池的商业化至关重要。
该工作以“Unique Tridentate Coordination Tailored Solvation Sheath Towards Highly Stable Lithium Metal Batteries”为题发表在期刊Advanced Materials上。第一作者为清华大学深圳国际研究生院博士研究生吴军茹。
研究亮点
(1)强调了溶剂分子与Li+络合方式,包括键长,静电势等差异性对溶剂化结构的影响。
(2)新型溶剂分子所造就的特征溶剂化结构——富阴离子,快速脱溶剂化等。
(3)在宽温条件下和极端工况下表现出优异的电化学性能。
图文导读
图1a、b显示了DME和BME分子等势面,当BME处于直链结构时,由亚甲基分隔的两个带有最负电荷的中间O原子有助于与Li+的络合。与Li+结合后,Li+-BME的键长为1.88 Å,比Li+-DME的长(图1d,e),表明BME对Li+的溶剂化能力较弱。在第二种状态下,BME分子是弯曲的,三个O原子强烈螯合Li+,这产生了一个新的三配位(图1c,f)。值得注意的是,Li+与弯曲的BME显示出不同的键长,分别为1.89 Å、1.91 Å和2.04 Å,与三个O原子。这些值比在Li+-DME配合物中观察到的键长要长得多,表明去溶化过程更加容易。在考虑阴离子后,基于DME的电解质的Li+-DME的平均键长为2.08 Å(标记为d1)。在LiFSI-BME电解质中,直链BME表现出与Li+的弱相互作用,Li+-BME的平均键长为2.11 Å(标记为d2,d2>d1)。相比之下,Li+和弯曲的BME之间较大的距离(平均2.36 Å,标记为d2',d2'>d2>d1)。这样的配位模式可以有效地将溶剂分子的立体阻碍作用发挥到极致,有利于溶剂化结构中阴离子聚集体的形成(图1g)
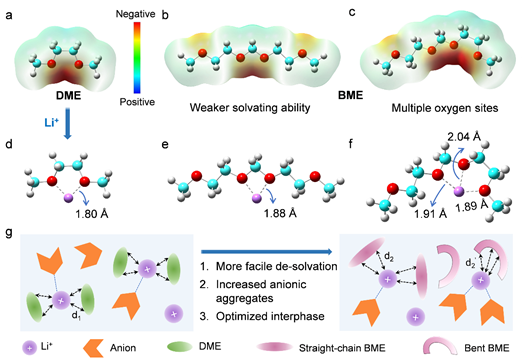
图1 分子设计。(a)DME和(b-c)BME溶剂的ESP。(c)Li+-DME和(d-e)Li+-BME的优化的结合几何学。(g) 基于DME和BME的电解质中Li+的溶剂化结构图。
图2的分子动力学(MD)显示在LiFSI-DME电解质中,内部的Li+溶剂化鞘层被FSI-和DME占据,显示了典型的CIPs(一个FSI-与一个Li+配位)。相比,LiFSI-BME电解质中观察到的Li+...O(FSI-)的峰值要高得多(图2b)。此外,在LiFSI-BME电解质中倾向于形成富FSI-阴离子参与的溶剂化结构。值得注意的是,弯曲的BME和Li+之间的三叉配位有助于FSI-阴离子在内部溶出鞘中占主导地位。电解质的溶剂化能(ΔGsolvation)、拉曼测试和核磁也证明了这一结果。即BME的弱溶剂化可以影响Li+的配位环境,从而促进LiFSI-BME电解液中产生富含阴离子的溶剂化结构。
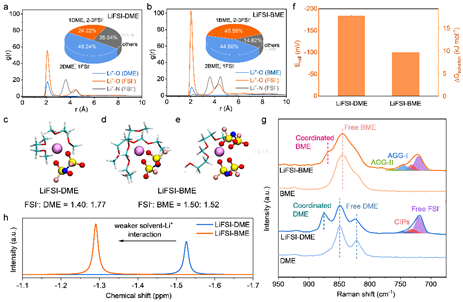
图2. 电解质的溶剂化结构。(a, b) 从(a) LiFSI-DME和(b) LiFSI-BME电解质的MD模拟得到的Li+径向分布函数。(c-e) (c)LiFSI-DME和(d, e)LiFSI-BME电解质的最可能的内溶剂化结构。(f)电解质的开路电压(Ecell)和相应的溶出能(ΔGsolvation)。(g) LiFSI-DME和LiFSI-BME电解质的拉曼光谱和 (h) 7Li NMR光谱。
如图3所示,LiFSI-BME电解质的Li+转移数(tLi+)为0.67,远远高于其他两种电解质(图3a)。这表明由于在迁移过程中容易脱溶,Li+在电解质中的扩散障碍小。同时,LiFSI-BME电解质的i0值和低的扩散能垒表明了富含阴离子的溶剂化鞘层极大地影响了SEI的结构和组成,赋予了Li+快速传输动力学以及快速的脱溶剂化动力学。值得注意的是,在LiFSI-BME电解液中,沉积的锂在宽温度范围内呈现出更紧凑、更均匀、更平整的状态。以上结果表明LiFSI-BME中的无树枝状和块状聚集的形态有效地减少了金属锂和电解质之间的有害寄生反应,这抑制了SEI的失控增长和死锂的形成,从而改善了电化学性能。
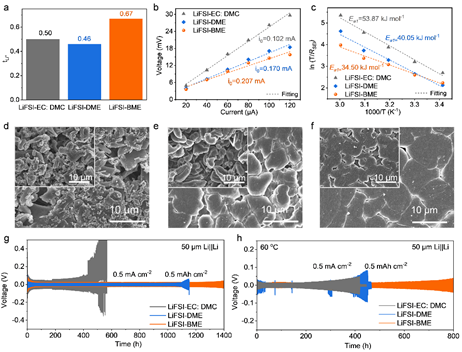
图3. 不同电解质中的动力学特性和Li沉积/溶解行为。(a) 室温下不同电解质中Li+的转移数。(b) 使用不同电解质的Li||Li电池进行Li沉积/溶解的交换电流密度(i0)。(c) 从不同电解质的循环Li||Li对称电池的Nyquist图中得出的RSEI的活化能。不同电解质的Li沉积的FE-SEM图像(d-f)60 ℃。插图中显示了25 ℃时Cu基片上的Li镀层形态的FE-SEM图像。(g, h) 不同电解质的Li||Li对称电池在(g)25 ℃和(h)60 ℃时的电压曲线。
图4a-d的TOF-SIMS可以看出,在LiFSI-BME电解液中形成的SEI要薄得多,由外部~5 nm的密集有机物层和~15纳米的无机LiF富集层组成。这说明大量的LiFSI参与了界面的形成。相应地,剖析深度显示,C2H-信号的强度在15s的溅射时间内急剧下降,而LiF2-的信号在30s的蚀刻后减弱到几乎为零。该结果通过XPS得到进一步验证,在LiFSI-BME电解液中形成的SEI中检测到更多的无机成分(LiF和Li2CO3),同时还有更薄的有机外层。总的来说,受益于富含阴离子的溶剂化鞘,LiFSI-BME电解液中的SEI层富含无机物,有助于促进均匀而致密的锂沉积行为。相反,LiFSI-DME和LiFSI-EC:DMC电解质的溶剂化结构中缺乏阴离子,导致有机SEI层的形成,从而难以抑制枝晶的生长、死锂的形成和电解质的消耗。
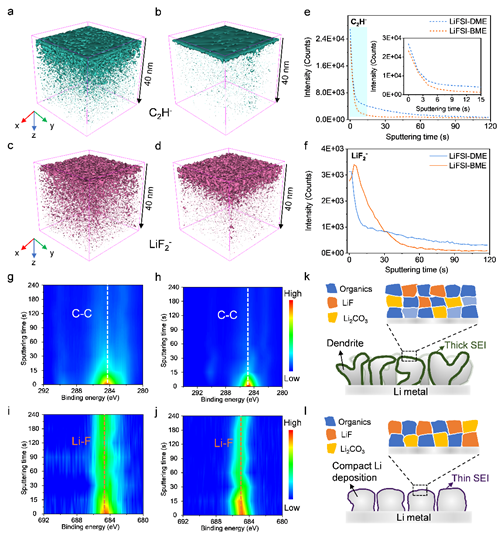
图4. 金属锂负极的界面化学。(a-d) C2H-和LiF2-的三维重建分布图,显示了从使用(a, c) LiFSI-DME和(b, d) LiFSI-BME电解质的循环Li||Li电池中获取的SEI结构和化学成分。(e, f) (c)C2H-和(f)LiF2-的相应强度溅射曲线。(g, h) 在(g, i) LiFSI-DME和(h, j) LiFSI-BME电解质中,在锂金属负极上形成的SEI层的C 1s和(i, j) F 1s XPS深度光谱。(k, i) 在(k)LiFSI-DME和(i)LiFSI-BME电解液中的锂沉积行为和SEI形成示意图。
图5a显示了在1℃下电池的长期循环性能。使用LiFSI-BME电解质的电池在1400次循环后保持80%的容量保留,平均CE高达99.8%。且其表现出良好的倍率性能(图5b,c)。同时,在具有高容量LiFePO4(1.8 mAh cm-2)和50 μm薄的Li箔的电池(图5d),LiFSI-BME电解液在500次循环中对Li||LiFePO4电池实现了92%的高容量保持率和99.93%的高度稳定的CE,表明形成了强大的SEI和明显抑制了Li消耗。采用LiFSI-BME的电池的性能优势可以通过小的界面阻抗(RSEI和Rct)和相应的电阻变化(图5e)进一步验证。此外,使用LiFSI-BME电解质,LMB表现出卓越的宽温性(图5f-g)。
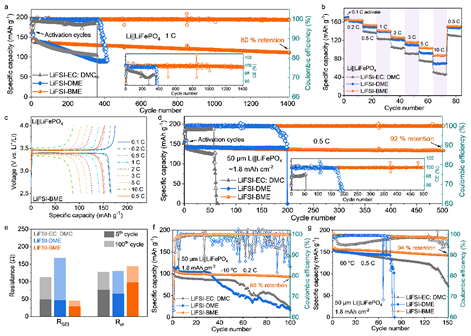
图5. LMBs的电化学性能。(a) 室温下1 ℃的Li||LiFePO4电池的长期循环性能。(b) 不同倍率速率下Li||LiFePO4电池的速率性能。(c) 使用LiFSI-BME电解质的Li||LiFePO4电池在不同C速率下的充放电电压曲线。(d) 50 µm Li||高负载LiFePO4电池在0.5 ℃下的循环性能。(e) Li||LiFePO4电池在5和100次循环后的拟合RSEI/Rct电阻值。(f, g) 50 µm Li||高负载LiFePO4电池在(f)-10 ℃和(g)60 ℃下的循环性能。
通过组装负极(10 mAh cm-2)和正极(2.87 mAh cm-2),面积容量比(N/P)为3.5的软包电池,进一步证明了BME的实际应用价值。使用LiFSI-BME电解液的Li||LiFePO4软包电池表现出更强的稳定性,100次循环后容量保持率达到99.5%(图6a)。同时,循环后的电池在形状上没有明显的变化(图6d),而其他系统则以严重的肿胀而失败(图6b,c),为了非破坏性地观察锂金属负极在循环后的形态,对循环的软包电池进行了X射线计算机断层扫描(X射线CT)(图6e-g)。在LiFSI-BME电解液中循环的小袋电池的锂阳极仍然保持金属光泽,没有出现枝晶和锂粉化的现象,表明电解液与锂负极的兼容性良好,从而大大抑制了寄生反应(图6g),对最先进的基于LiFePO4的LMBs的概述突出了LiFSI-BME电解液的优越性,与先前报道的电解液体系相比具有相当的竞争力(图6h)。
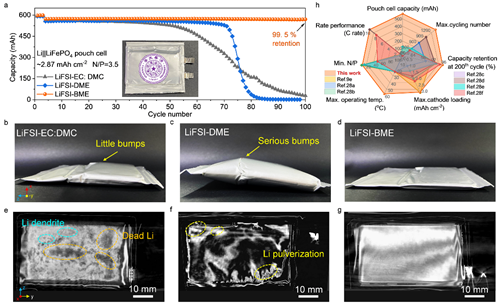
图6. 软包电池的性能和特征。(a) 使用不同电解质的Li||LiFePO4软包电池的循环性能,设计容量为570 mAh。插图显示了一个软包电池的数字图像。(b-d)使用(b)LiFSI-EC:DMC、(c)LiFSI-DME和(d)LiFSI-BME电解质的小袋电池在100次循环后的光学图像。(e-g)使用(e)LiFSI-EC:DMC、(f)LiFSI-DME和(g)LiFSI-BME电解质的软包电池的X射线CT图像。(h) 倍率性能、最小N/P比、最大工作温度(℃)、最大正极负载(mAh cm-2)、第200次循环时的容量保持率(%)、最大循环次数和软包电池容量(mAh)等参数的比较。
总结与展望
综上所述,通过合理的溶剂分子设计,提出了一种具有多个氧位点的新型溶剂,以提供独特的Li+的双/三配位螯合物。在浓度为1.0 M的单一盐和唯一的BME溶剂中实现了富含阴离子的Li+溶剂化鞘,表现良好的Li金属兼容性和快速的脱溶剂化动力学。LiFSI-BME电解质在50 µm的对称锂电池中表现出1400小时的寿命,在-10 ℃、25 ℃和60 ℃的不同温度下表现出紧凑的锂沉积。使用50 μm-Li负极和1.8 mAh cm-2的LiFePO4正极的全电池在500次循环中保持稳定,容量保持率高达92%,平均CE为99.93%。此外,在-10 ℃至60 ℃的宽温度范围内工作的电池和工业上百毫安时的软包电池的循环稳定性也得到了明显的改善,显示了商业应用的巨大潜力。这项工作代表了分子设计策略的重大进展,促使人们对下一代LMBs的电解质优化进行深入研究。
审核编辑:刘清
-
锂离子电池
+关注
关注
85文章
3234浏览量
77677 -
电解质
+关注
关注
6文章
810浏览量
20045 -
ESP
+关注
关注
0文章
183浏览量
33918 -
DME
+关注
关注
0文章
22浏览量
7411 -
锂金属电池
+关注
关注
0文章
135浏览量
4311
原文标题:独特的双/三鳌合方式!清华大学李宝华教授和昆明理工大学王贤树特聘教授AM: 单溶剂分子特殊的络合方式,调控阴离子溶剂化结构
文章出处:【微信号:清新电源,微信公众号:清新电源】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
离子液体添加剂用于高压无负极锂金属电池

钾离子辅助的多阴离子材料—钠离子电池长循环稳定性的新机制

武汉理工大学在水系锌离子电池研究方面取得新进展
谁能帮忙设计 让蜂鸣器的声音更大?费用大概多少?
稳石氢能中标全球首套单系统1.25MW阴离子交换膜电解水制氢项目!

新宙邦美国路易斯安那州碳酸酯溶剂和锂离子电池电解液项目启动
用于单分子无标记定量检测的数字胶体增强拉曼光谱技术

基于量子干涉技术的单分子晶体管问世
弱溶剂化少层碳界面实现硬碳负极的高首效和稳定循环





 单溶剂分子特殊的络合方式,调控阴离子溶剂化结构
单溶剂分子特殊的络合方式,调控阴离子溶剂化结构














评论