皮肤间质液(ISF)是一种丰富的生物标记物来源,是对血液和尿液等传统生物流体的补充。它含有重要的代谢和免疫生物分子,并与血液密切相关,因此有望取代目前基于血液的金标准诊断。与血液相比,ISF具有多种优势,包括可通过皮肤广泛获取、可采用无创或微创采样方法以及凝血因子的部分存在,因此有利于对生物标记物进行连续监测。多项研究表明,ISF、血清和血浆的成分相似,尤其是葡萄糖、尿素、乳酸盐、H⁺(pH 值)、Na⁺、K⁺等低分子量物质,尽管ISF的可及性似乎很高,其体积是血液的三倍,但采集ISF样品仍是一项具有挑战性的任务。近年来,能以无痛、易用的方式提取真皮层ISF的微针可穿戴装置越来越受到关注。
近期,来自土耳其科奇大学(Koç University)的Levent Beker团队介绍了一种基于激光钻孔空心微针(HMN)贴片的全集成触摸激活式可穿戴装置,可用于连续采样和检测真皮层ISF。所开发的真空集成ISF提取和传感(VIES)平台可产生并维持所需的真空压力(低至约-53 kPa),以收集足够量的ISF(~ 2 μL/针/h),可用于医疗应用。真空系统可通过手指一触式操作启动。对微针阵列大小、真空压力和抽取持续时间对收集到的ISF的影响进行了参数研究。通过对动物模型中ISF的葡萄糖和pH值进行电化学检测,进一步证明了所提议的平台具有连续健康监测的能力。这种基于激光钻孔空心微针的系统为医疗诊断和治疗提供了一种替代现有侵入性ISF收集和传感技术的工具。相关工作以题为“A Wearable Touch-Activated Device Integrated with Hollow Microneedles for Continuous Sampling And Sensing of Dermal Interstitial Fluid”的文章发表在国际著名期刊Advanced Materials上。
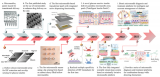
该VIES系统由四部分组成,包括:(a)真空发生室和液体萃取室;(b)集成丝网印刷电极的三维柔性微流控模块,用于ISF采样和传感;(c)激光钻孔空心微针补丁;以及(d)自主开发的印刷电路板,用于信号采集和通过蓝牙模块进行数据传输。图1a展示了可穿戴VIES装置,该装置安装在人体手臂上,用于ISF采样和现场ISF分析。图1b展示了VIES系统三个主要部分的特写图。测量数据可通过向电子设备无线传输电化学传感信号来获取(图1c)。如图1d所示,微流控模块是由双面胶带、带有丝网印刷电极的透明PET薄膜、空心微针贴片和皮肤粘合剂垂直组装而成。如图1f所示,真空发生系统由三个主要部分组成:(1)真空发生室;(2)液体提取室;(3)被动(单向)阀。用手指按压真空室可激活出口被动阀(CV #1),而两个真空室之间的阀门(CV #2)则保持关闭状态。这就在腔室中产生了负压,由于已建立的压力梯度,打开了CV #2,关闭了CV #1(图1g)。当液体吸收室和真空发生室达到平衡压力时,两个被动阀都会关闭,因为与大气压力相比,腔室的压力较低。产生的负压有助于通过空心微针将ISF抽取到微流控室内(图1h、1i)。使用CV #2 可以连续按压真空发生腔,而不会降低液体提取腔的真空压力。图1j、1k是使用VIES系统提取ISF的示意图。
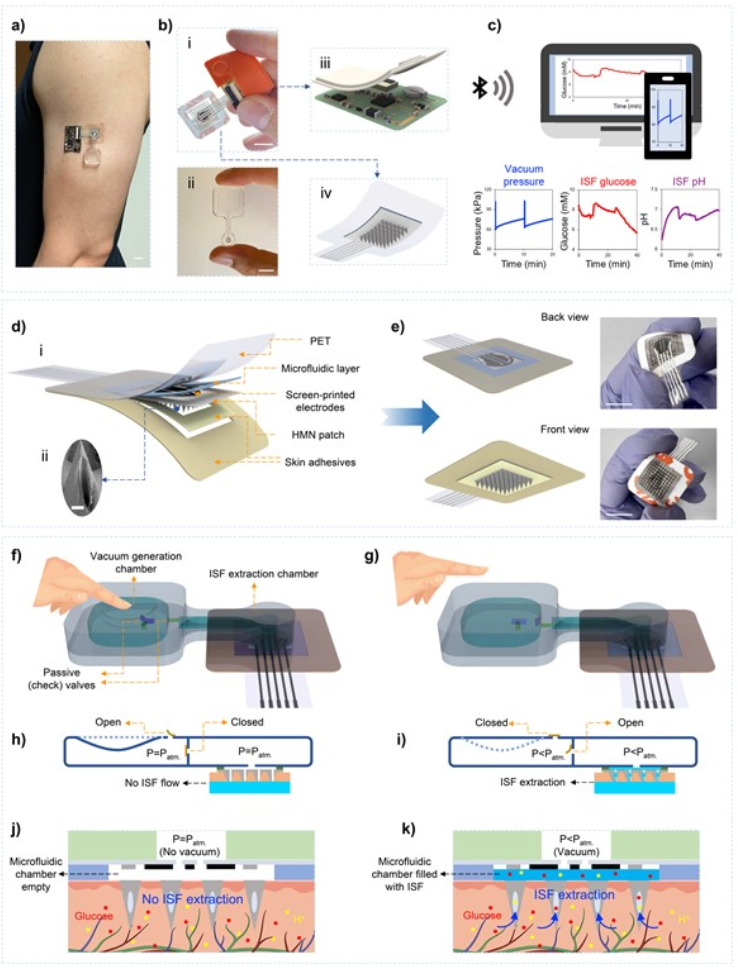
图1 基于空心微针的按需提取ISF和电化学传感的可穿戴装置图解
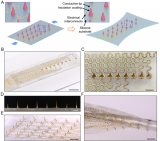
空心微针贴片采用传统的成型技术制备,然后用激光钻针建立从皮肤到微流室的ISF传输微通道。微针贴片由金字塔形的微针组成,其高度、边缘宽度和金字塔中心之间的空间分别为1.5毫米、0.6毫米和1.2毫米(图2)。图2b给出了微针补丁的详细形态特征,这些特征分别用光学显微镜和扫描电子显微镜(SEM)观察到。为了最大限度地降低组织堵塞造成的堵塞风险,空心微针设计为侧面开口,开口朝向垂直于插入方向,而不是针尖上的开口。为了研究微针的机械强度,本研究按照以前报道过的方案,使用了定制的力-位移测试装置。压缩研究(图2e)证实了微针补丁的机械稳定性,因为没有观察到断裂(曲线平滑,图中的力没有急剧下降)。由此产生的针尖末端垂直位移约为0.15毫米(约为针高的10%,n = 3),因此对微针贴片的穿透性能影响很小。插入研究表明,要达到1.5毫米的位移(相当于微针的长度)需要不到2牛顿的压力(每针0.08牛顿,n = 3)。需要注意的是,由于皮肤具有弹性,针刺入皮肤的深度将低于1.5毫米。在剪切载荷试验中,将每根针刺入皮肤的力减小到2牛顿(与压缩载荷类似),得到了一条平滑的曲线,并观察到轻微的位移,这表明微针贴片的结构保持完整。
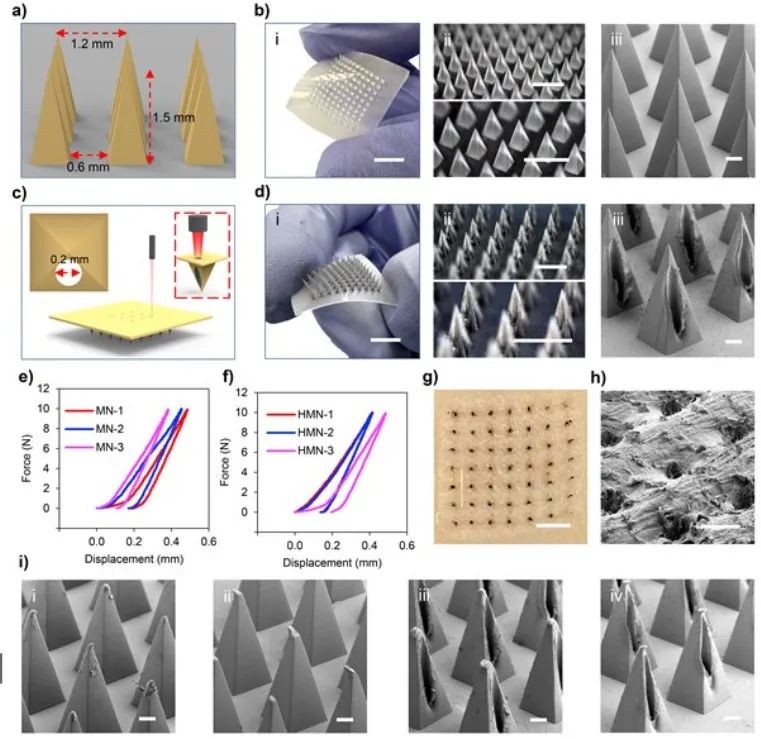
图2 微针和空心微针贴片的表征
本研究在每个腔室(真空发生腔室(CH #1)和ISF抽取腔室(CH #2))内放置了压力传感器,以便在表征实验过程中监测压力曲线。如图 3a(i)所示,由于CH #1内部压力增加,对CH #1施加压缩力会激活CV #1。消除压缩力后,基于PDMS的CH #1的弹性自我恢复导致腔内压力下降,从而激活CV #2,以平衡两腔之间的压力。当两个腔室内都达到负表压时,CV #1和CV #2都会闭合,CH #2内的真空压力将成为从皮肤中提取ISF的驱动力。
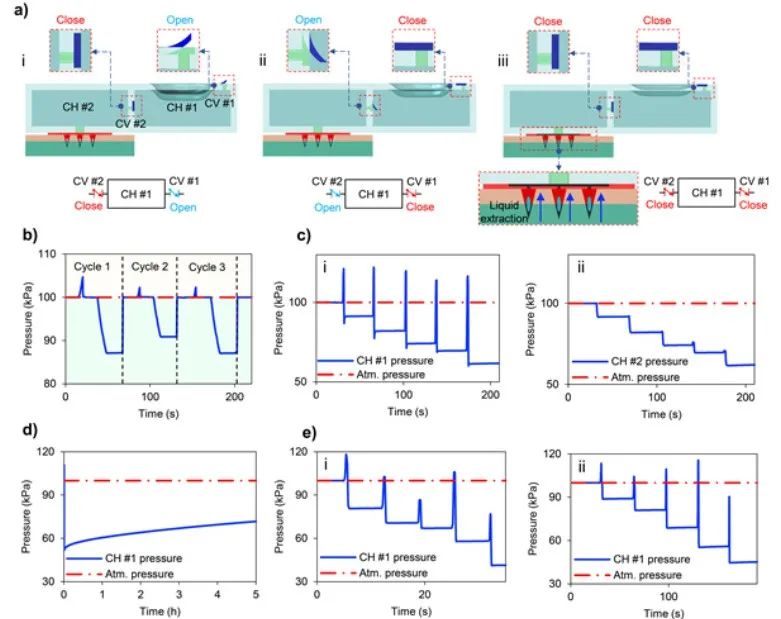
图3 ISF抽出系统的性能表征
为了评估葡萄糖传感器的灵敏度,本研究首先在20 μM至1 mM的葡萄糖浓度范围内对传感器的性能进行了校准。在葡萄糖浓度较低(20 μM ~ 1000 μM)时,电极的灵敏度和检测限(LOD = 3.3 σ/S,其中σ为传感器响应的标准偏差,S为校准曲线的斜率)分别为0.254 μA/mM和5.6 μM。如图4a、b所示,测量到的传感器响应随葡萄糖的添加而增加,呈现线性趋势,相关系数为0.98,可进一步用于获得校准曲线(图4c)。结果表明,葡萄糖传感器可以满足葡萄糖监测的要求,其检测范围可以覆盖人体血液中的正常葡萄糖水平(约4.4 mM ~ 6.6 mM),这实际上与ISF葡萄糖水平相同。在葡萄糖浓度为100 μM和5 mM时,测量电流的相对标准偏差(RSD)分别为1.22%和2.57%,表明传感器具有可靠的检测一致性。此外,传感器在储存七天后的功能偏差(RSD为2.9%)可忽略不计,这反映了酶固定的稳健性。
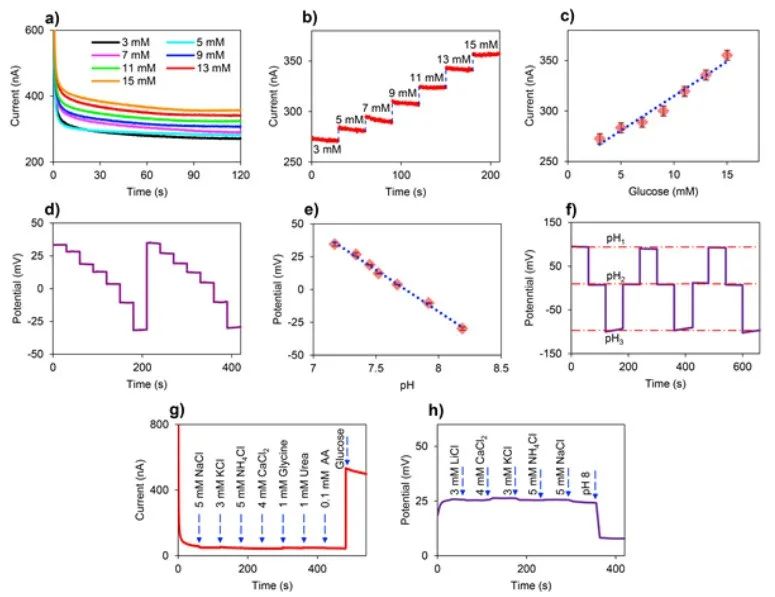
图4 电化学传感器的实验表征
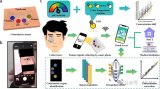
在进行体内实验之前,本研究通过使用体外皮肤模型(模拟设想的ISF采集和生物传感场景)扩展了VIES系统在ISF提取和传感方面的特性。图5a是用于活体外试验的实验装置示意图。为评估VIES系统的ISF提取能力,本研究将空心微针贴片按压在新鲜皮肤样本上,并将染有蓝色染料的滤纸放入微流控室内以方便观察,同时使用专用压力传感器监测真空发生系统内的压力。如图5b所示,在最初的10分钟内,几乎没有液体进入微流控室。大约17分钟后,ISF开始通过针头上的微通道流向腔室。ISF流经微通道的延迟源于PC微针的疏水性。这个问题可以通过等离子处理得到部分解决,等离子处理会导致接触角减小。但是,这种方法的主要问题是聚合物的疏水性会随着时间的推移而恢复,因此这种方法不适用于连续监测装置和使用前需要储存一段时间的装置。在真空条件下,由于体内外实验中没有ISF负压,ISF在克服通道疏水性产生的流体动力阻力后很容易流过空心微针。
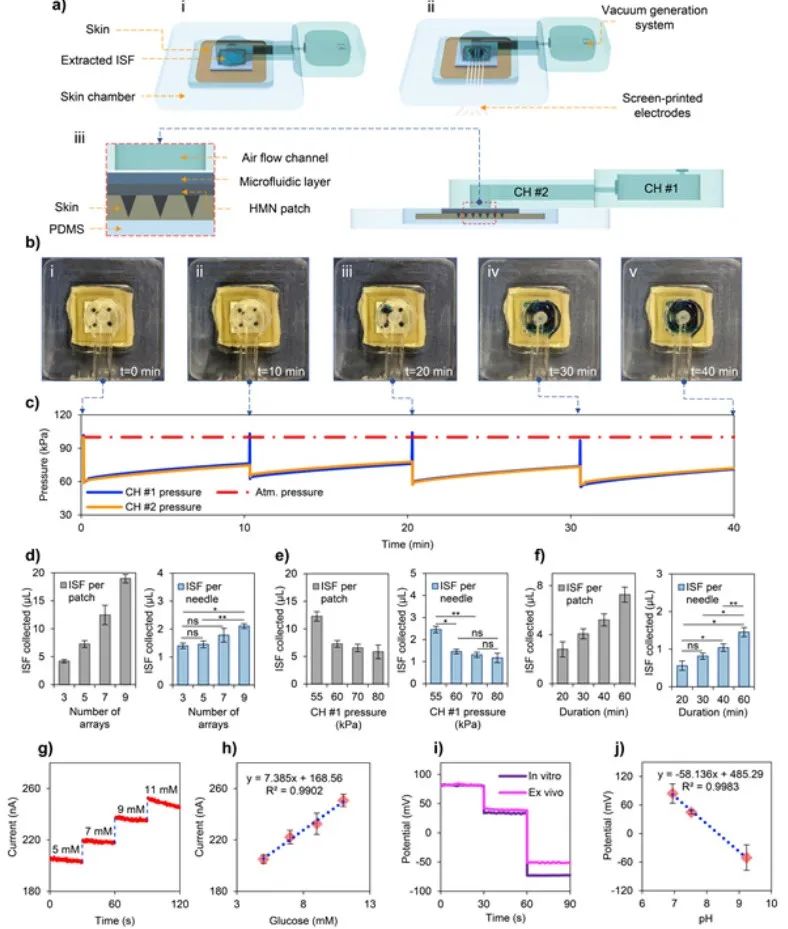
图5 VIES系统的离体表征
如图6所示,与体内外实验类似,由于聚合物微通道的疏水性,一开始提取 ISF的速率非常低。大约16分钟后,真空压力超过了疏水性压力屏障,ISF开始以更高的速率流入微流控室内。在体外实验中,ISF在提取开始后几分钟内就充满了微流控室;而在体内实验中,ISF需要更长的时间才能充满微流控室。这可能是因为在活体动物模型中ISF存在负压,对ISF的提取产生了额外的阻力。从图6b中可以看出,在收集的ISF样品中没有观察到血液。根据以前的研究,真空给药后延迟提取ISF有利于避免血液污染。通过比较图5d、5e、5f 和图6c、6d、6e中分别对应体内外实验的数据,可以看出体内实验的ISF收集率较低。其中一个原因可能是记录了一小时的ISF采集率。
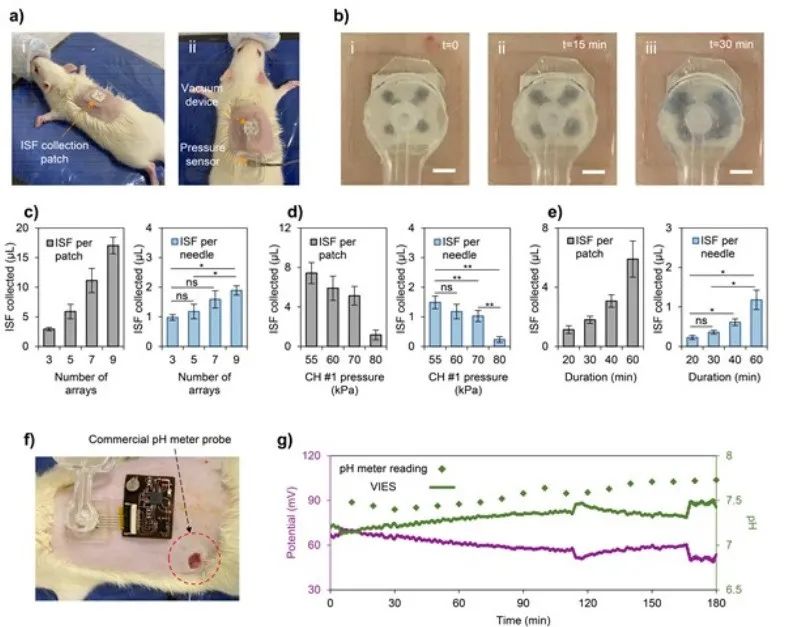
图6 基于空心微针的VIES系统的体内ISF采集和传感性能
综上所述,本研究开发了一种可穿戴的真空集成ISF提取和传感装置,利用空心微针连续收集ISF。本研究制作了一种激光钻孔聚合物空心微针贴片,可以轻松穿透皮肤并提取ISF。真空系统的特性研究表明,该系统能够产生并维持足够的真空压力,以进行ISF采样。参数研究表明,增加空心微针的数量和提高真空压力会极大地影响ISF的收集量。VIES系统在大鼠模型上的成功应用表明,该装置能够通过简单的手指单触操作即可提取足够量的 ISF。本研究提出的装置具有简单易用的ISF采集潜力,并能为将真空供电集成到基于ISF的可穿戴装置中铺平道路。
审核编辑:刘清
-
印刷电路板
+关注
关注
4文章
810浏览量
35470 -
激光器
+关注
关注
17文章
2579浏览量
60953 -
压力传感器
+关注
关注
35文章
2258浏览量
163816 -
SEM
+关注
关注
0文章
247浏览量
14582 -
传感技术
+关注
关注
5文章
539浏览量
46533
原文标题:集成空心微针的可穿戴触摸激活装置,用于皮肤间质液的连续采样和传感
文章出处:【微信号:Micro-Fluidics,微信公众号:微流控】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
加州理工学院:研究一种无创监测女性激素的可穿戴生物传感器
武汉松盛光电的一种控温激光装置专利:实时温度探测与反馈

用于3D脑血管成像和脑血流动力学监测的可穿戴超声贴片

半侵入式"可穿戴诊所"——微针技术的创新应用
PCB激光钻孔:精准之舞,铸就电子科技新高度
基于一种AI辅助可穿戴微流控比色传感器系统
#参考设计#可穿戴心电图设计方案

激光焊接技术在焊接医疗活检针的工艺应用

空心杯电机的结构原理是什么
适用于可穿戴设备和物联网的低IQ高度集成式电池充电管理解决方案BQ25121A数据表





 一种基于激光钻孔空心微针贴片的全集成触摸激活式可穿戴装置
一种基于激光钻孔空心微针贴片的全集成触摸激活式可穿戴装置











评论