近年来,软生物电子技术迎来了蓬勃发展的时代,因为它在个性化医疗监测、护理点临床诊断、假肢和人机界面等方面的应用前景广阔,将从根本上提高精确治疗学的效率,并改变人与机器的交互方式:(1)柔软、灵敏,可感知环境刺激的微小变化,如应变(0.1%)和压力(0.1%);(2)柔韧、可拉伸(~1000%),可顺应性地附着于任何弯曲表面,如人体皮肤;(3)薄(~1 um)、轻(3 g/m²),可实现难以察觉的集成和随时移动。这些突出特点使软生物电子器件能够与人体和假肢无缝集成,实现对各种物理和生物信息的实时、长期和低成本传感。迄今为止,已开发出多种软生物电子器件,包括电子皮肤、穿戴式传感器、柔性摩擦纳米发电机(TENGs)、软超级电容器和植入式电子器件。其应用范围很广,从触觉传感、重要生理信号监测、生物标志物检测(如汗液、泪液和尿液)到体内给药、细胞操作以及神经调控和治疗。传统器件无法实现的卓越功能已成功实现。例如,无电池表皮电子元件可用于无线、连续和实时测量脆弱新生儿的心电图(ECG)和光敏血压计(PPG)信号,与传统的硬连线监测系统相比,可大大减少对新生儿皮肤的伤害和对婴儿自然活动的限制。目前已发明了可植入的类组织电子元件,可与神经组织适形连接,通过电刺激实现局部神经调控。
尽管软生物电子学正在为人类生活和社会带来快速变革,但目前开发的生物电子学大多基于纺织品等具有较大杨氏模量(通常为2 Mpa ~ 1 GPa)和非内在生物相容性的材料,与人体皮肤或组织的机械不匹配以及严重的生物相容性问题极大地阻碍了它们在生物医学领域的实际应用。与这些材料相比,水凝胶是一种渗入大量水分(80 wt%)的三维聚合物网络,因其具有模拟组织的杨氏模量、优异的生物相容性与生物相似的离子导电性和多种刺激响应性,已被广泛认为是开发生物医学应用领域软性穿戴式和植入式电子器件的理想材料。具体来说,水凝胶的杨氏模量(~1 Pa至~1 MPa)与人体皮肤或组织的杨氏模量(~1 kPa至~100 kPa)接近,可使电子组织界面具有极佳的机械匹配性,有助于实现电子与生物的顺应性集成。其优越的细胞外基质仿生结构使软生物电子器件具有类似原生组织的生理特性,即良好的细胞相容性和组织相容性可避免在长期附着过程中出现意外的生物免疫反应。同时,水凝胶的离子传导机制使电子器件能够与生物组织进行便捷的电交流。因此,水凝胶电子器件可以在机械、电学和生物化学特性等各个方面完美地弥补人类与机器之间的差距,并实现下一代软生物电子学的开发。迄今为止,已开发出多种基于水凝胶的软生物电子器件,包括传感器、显示器、TENGs和植入式电极,可用于皮肤和植入式应用。
尽管水凝胶在开发穿戴式和植入式生物电子器件方面前景广阔,但在临床过渡和实际应用之前,仍存在一些挑战性问题,需要加以解决。其中一个关键挑战是,由于水凝胶固有的杨氏模量较低,加上人体内复杂的承载和动态环境,水凝胶生物电子器件在使用过程中很容易损坏,这严重阻碍了其长期可靠的应用。例如,穿戴式电子器件不可避免地会受到来自外部环境的各种机械力的影响,如划痕、磨损、撕裂和穿刺。在人体器官和关节频繁而持续的运动过程中,如心脏的持续收缩和扩张,植入式生物电子器件可能会受到超范围拉伸、应力疲劳和应力引起的内部微裂缝的破坏。
人的皮肤是一种复杂的感官系统,在受损时可以再生或修复,因此可以工作一百多年。受此启发,研究人员致力于赋予水凝胶生物电子“自再生”或自修复“能力,以延长其耐用性、可靠性和寿命。自愈能力在软生物电子学中发挥着重要作用,因为它可以从根本上克服软生物电子学在运行过程中不可避免的结构断裂和功能失效或退化。其基本机理是,具有自愈合能力的水凝胶(SHHs)能够在受损后重建断裂的键,从而恢复其原有的机械、化学和电子特性。这种能力赋予了水凝胶软生物电子学几种显著的功能:(1)使软生物电子器件在受到破坏后能够恢复其原有的结构、功能和性能;(2)通过应力消散效应提高器件的机械耐久性,以实现长期应用,当受到负载时,自愈合水凝胶中的可逆动态键可作为牺牲键断裂并消散累积的应力和能量,从而减轻应力集中和对结构的破坏。当载荷移除时,断裂的可逆键可以重塑,恢复受损水凝胶的原始结构和机械性能,从而抵御应力引起的裂缝和应力疲劳,提高器件的机械耐久性。(3)赋予软生物电子器件形状适应能力,即通过自愈合水凝胶中可逆链接的断裂和重构,使其结构适应各种组织或器官形状。
近期,Advanced Materials期刊发表了题为“Self-healing Hydrogel Bioelectronics”的综述,讨论了自愈合水凝胶的最新进展,从水凝胶材料的自愈合机理、材料化学和多种性能改进策略,到各种基于水凝胶的生物电子器件的设计、制造和应用,包括穿戴式物理和生化传感器、超级电容器、柔性显示器件、摩擦纳米发电机(TENGs)、植入式生物电子器件等。此外,还提出了阻碍自愈合水凝胶生物电子学发展的持续挑战及其前景。该综述有望加快自愈合水凝胶在各种自愈合生物电子学中的研究和应用。香港大学张世明教授及西安交通大学赵立波教授、西北工业大学薛语萌教授为共同通讯作者。
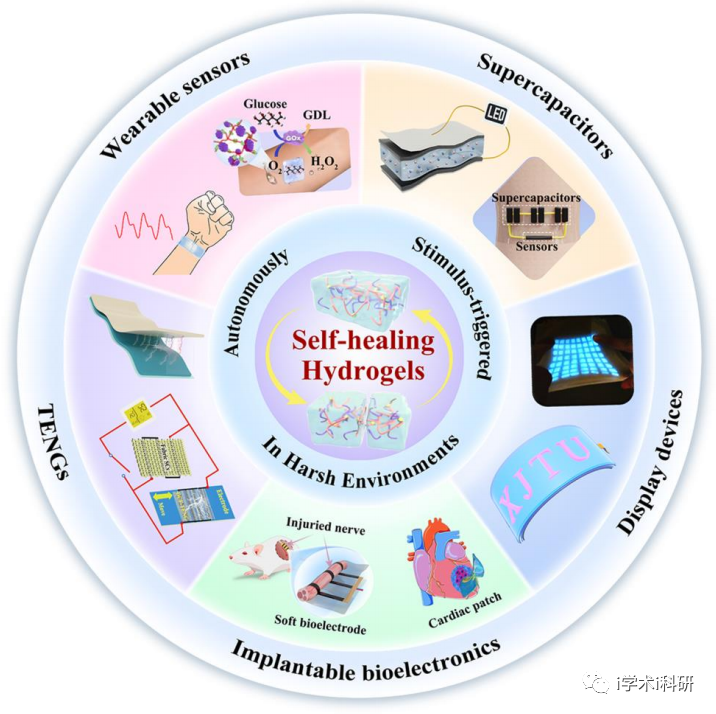
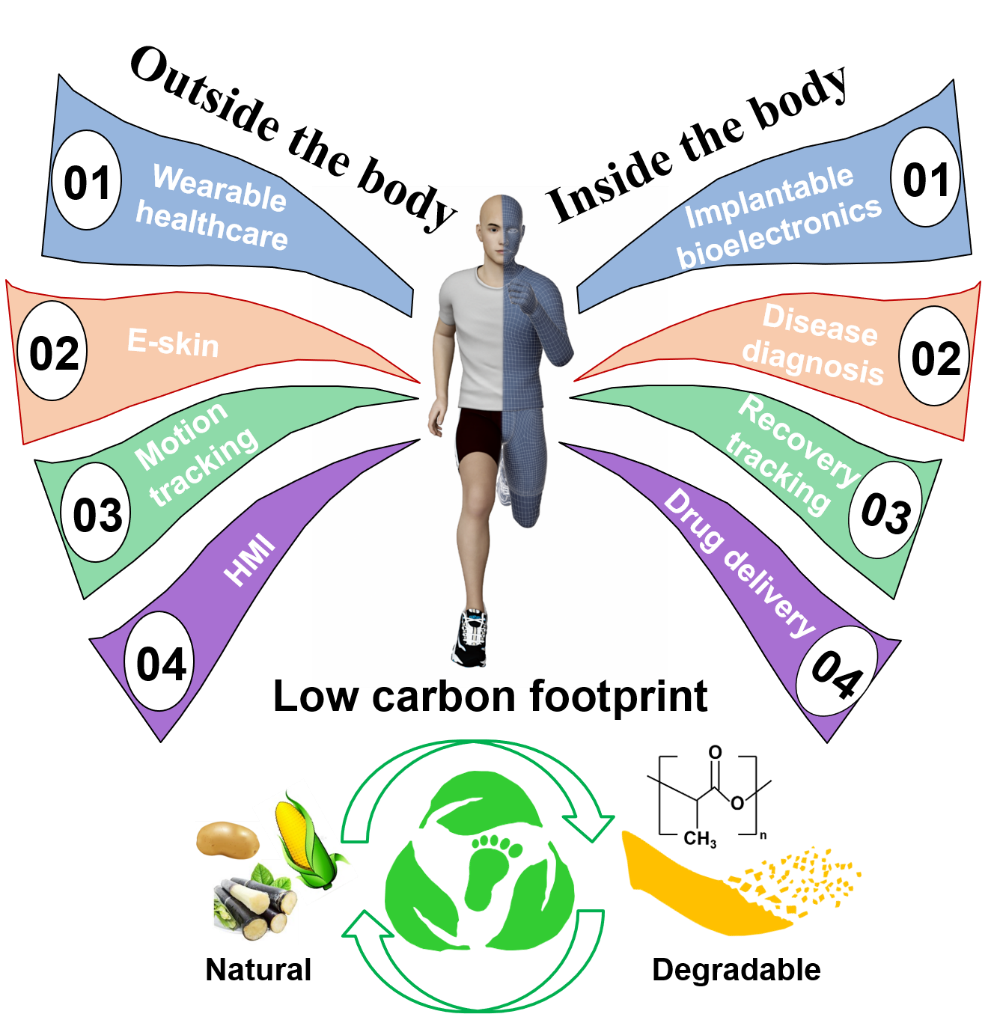
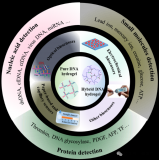
自愈合水凝胶的原理图及其在软生物电子学中的潜在应用
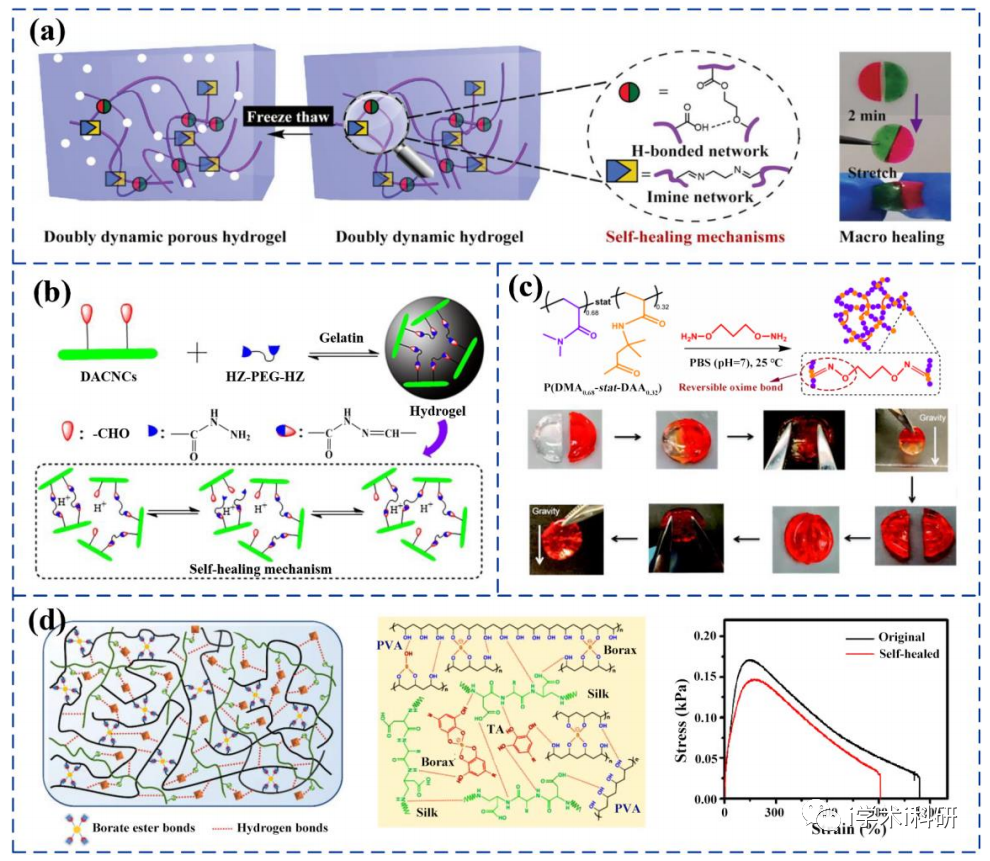
基于动态共价键相互作用的自愈合水凝胶
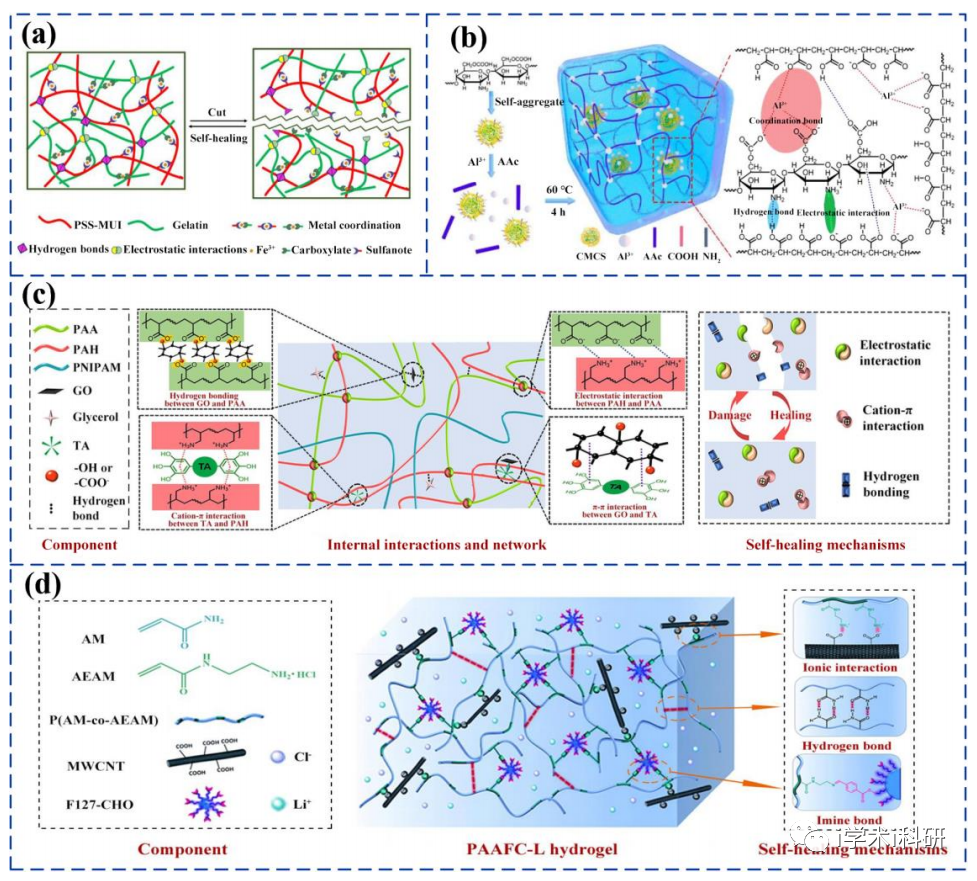
基于多种协同性相互作用的自愈合水凝胶
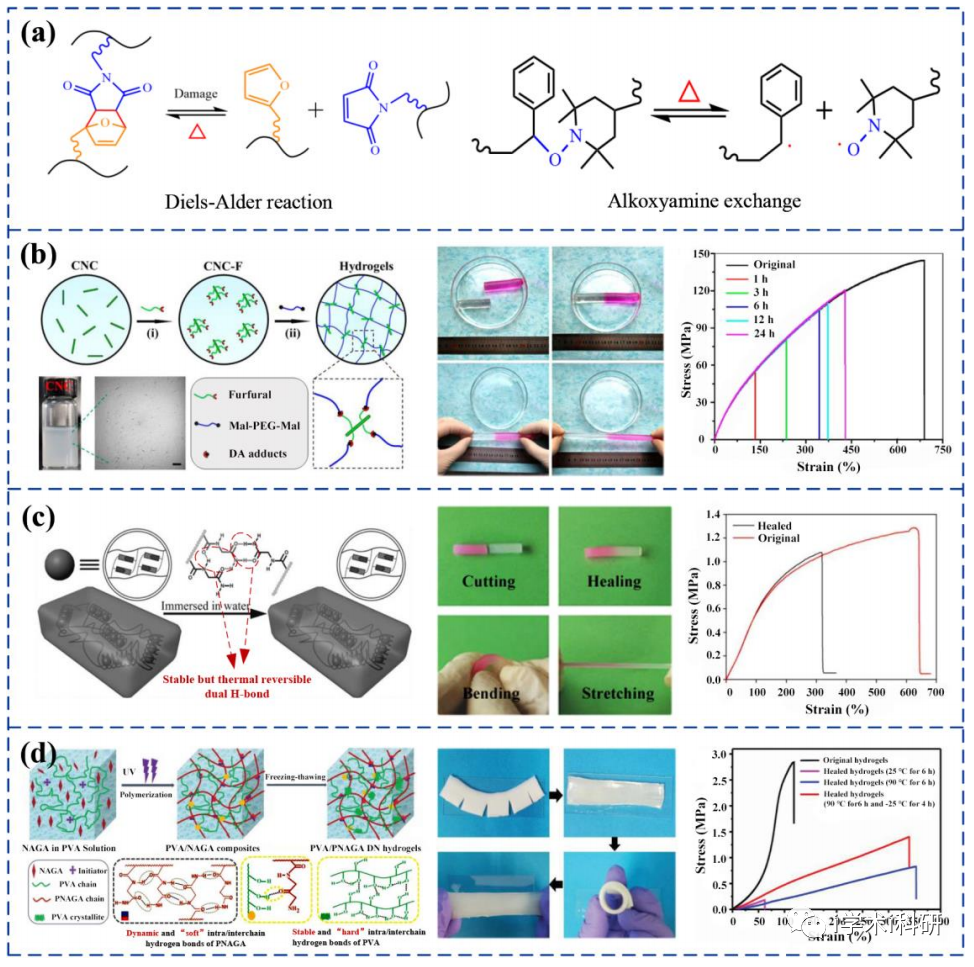
热触发自愈机制及制备的自愈合水凝胶
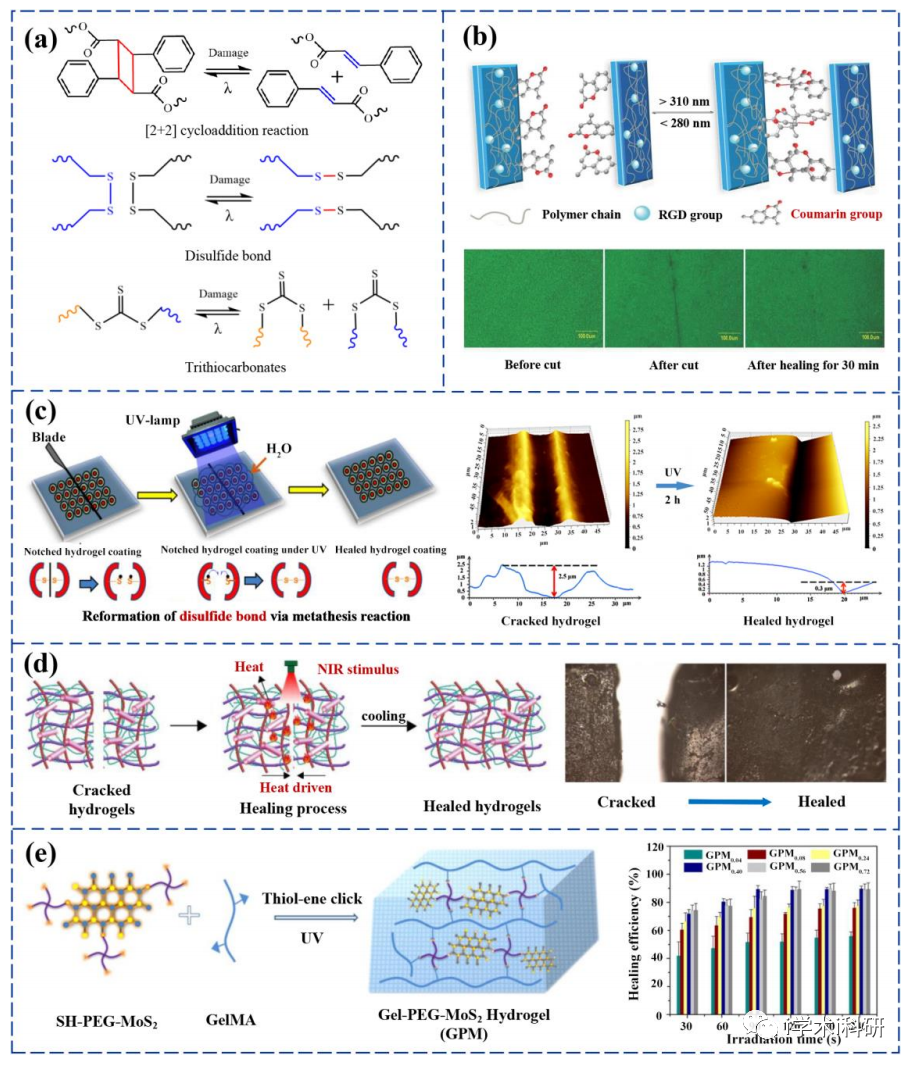
光触发自愈机制及制备的自愈合水凝胶
在这篇综述中,作者重点介绍了过去几年在合成自愈合水凝胶及其应用于开发软生物电子学方面所探索的最突出机制。目前已构建出多种自愈机制,涉及自主和外部刺激响应特性。利用这些机制,许多自愈合水凝胶得到了证实,它们在自愈率、恢复速度、允许的自愈周期以及许多其他理化性能(如机械强度、伸展性、导电性、抗冻能力、保水性能等)方面都有显著改善。这些自愈合水凝胶的应用范围很广,从穿戴式传感器、光学显示器、超级电容器和TENG到植入式生物电子器件。机械损伤后出色的性能恢复能力已得到证实,从而大大提高了软电子器件的可重复使用性和使用寿命。尽管已经取得了巨大进步但大多数已开发的自修复电子器件仍处于概念验证阶段。在最终的工程应用之前,还需要应对巨大的挑战。
(1)深入了解自愈合理论和性能评估。目前,大多数研究工作都集中在探索水凝胶可能的自愈合机制,并通过实验证明其宏观自愈合行为。目前还缺乏分子层面的自愈合动力学理论分析或建模,无法说明分子的类型、动力学和浓度以及环境参数(如温度、pH 值等)对动态键的形成以及键能的影响。建立理论模型,从分子成分定量计算水凝胶的自愈合宏观性能(例如自愈合效率、时间和周期)是可取的。这些模型不仅能预测给定条件下的自愈合性能,还能在机器学习和人工智能的帮助下提供强大的设计策略,以满足目标容量要求。此外,构建性能评估标准和相应的实验表征方法也将有助于直接定量表征和验证水凝胶的自愈合性能。
(2)同时提高自愈合能力和其他所需的材料性能。在软电子器件的实际应用中,水凝胶不仅要具备自愈合能力,还要具备许多其他必要的性能,如机械强度、拉伸性、导电性等。然而,由于这些性能对材料组件设计的要求相互矛盾,因此在同时提高这些性能方面存在巨大挑战。一个常见的挑战是如何权衡自愈合水凝胶与机械性能(杨模量)之间的关系。具有高自愈合能力的水凝胶在环境温度下很少有足够的杨氏模量。这是因为高杨氏模量需要快速的段和链动力学以及易于断裂/交换的动态键,而这通常是以低模量和弱动态键的聚合物链为代价的。探索新策略来平衡包括自愈能力在内的多种功能之间的矛盾,对于实现水凝胶的实际工程应用至关重要。一个有前景的解决方案是利用结合了不同动态键的复杂分子设计和具有特定形态的网络结构。
(3)赋予自愈合水凝胶环境适应能力。由于水凝胶具有富水和亲水性,因此在环境温度或更高温度下容易脱水,在低温下容易冻结,在水中容易膨胀。这些因素会降低水凝胶电子器件的稳定性和可靠性,甚至导致器件失效。在确保自愈合性能的前提下,解决失水、冻结和膨胀问题对自愈合水凝胶电子器件至关重要,这可以提高器件的稳定性和可靠性,扩大其应用范围,如在低温、水下等环境下。此外,具有可控降解性的自愈合水凝胶在开发环境友好型植入式自愈合软器件方面也大有可为。
(4)开发具有完全自愈能力的软电子器件。尽管过去几年中已经展示了多种自愈合软电子器件但很少有器件能实现整体自愈合,尤其是那些具有多层或多层结构元件的器件,如电容式传感器。要实现完整的自愈合水凝胶电子器件,器件结构的每个元件层都应具备自愈合能力。也就是说,除了水凝胶外,器件结构所需的许多其他材料也应具有自愈合能力。此外,由于自愈合性能(速度、重复周期和条件)的不匹配,在器件愈合过程中克服功能失效引起的变形、剥离和错位更具挑战性。针对这一问题,应大力构建有效的策略。此外,不同层之间的界面粘附/粘合和界面自愈也有助于保持器件结构的稳健性,并在损坏后实现全面的性能恢复。
(5)探索自愈合水凝胶电子器件的制造技术。制造技术是开发自愈合水凝胶电子器件的关键。它弥补了器件概念与实际应用之间的差距。目前,大多数基于自愈合水凝胶的电子器件都是用结构设计简单的块状自愈合水凝胶制造的,而且图案化和集成都是人工进行的。当务之急是探索能实现图形图案化、器件间一致性和集成制造的制造技术。在这方面,3D/4D打印、软光刻、丝网印刷、直接墨水书写和喷墨打印在制造具有复杂结构和一致性能的自修复水凝胶电子器件方面具有巨大潜力。此外,微型化和可扩展制造可缩小器件尺寸,实现高密度集成(使单个器件具有多种功能),并降低成本,而这正是自愈合软电子器件所急需的。制造具有微/纳米厚度和良好透气性的自愈合水凝胶器件可提高用户长期使用的舒适度。
(6)赋予自愈合水凝胶生物电子学新功能,实现更广泛和革命性的应用。随着基于自愈合水凝胶的柔性电子技术深入人类生活,需要不断赋予其新的革命性功能,以拓展应用范围,创新现有应用方式。例如,具有形状记忆功能的自愈合水凝胶生物电子器件可以记忆复杂的形状并在外部刺激下以可编程的方式恢复到初始形状,可广泛应用于微创手术、生物医学器件和智能软生物致动器等需要器件结构和性能具有可控激活能力的场合。自愈合水凝胶电子器件具有形状可编辑和自粘附能力,可以保形粘附在所需形状的组织或复杂器官表面,实现长期生理信息监测,并进一步应用于人工神经、脑机接口和脑疾病治疗。此外,自愈合水凝胶电子器件还可以与自愈合超级电容器和自愈合TENGs集成,实现自供电,从而实现连续运行。例如,集成的自愈式穿戴式传感器可实现连续、长期、穿戴式的医疗监测,而这正是柔性电子技术发展的最终目标。
一旦攻克了这些关键难题,通过合理地结合多种自修复机制和拓扑结构设计,将有望构建出具有卓越综合性能的自修复水凝胶。自愈合水凝胶生物电子器件将能在成千上万次的损伤下完全恢复其性能,并同时具备许多其他优异性能,如足够的机械强度、高拉伸性、优异的导电性、理想的稳定性和可靠性等。随着自愈合水凝胶生物电子学的快速发展,其在穿戴式生理信号监测、体内给药、组织工程支架、人体器官电生理信号传感、伤口包扎、隐形眼镜、神经信号记录与调控、重大神经疾病治疗等领域均已实现临床转化或商业化。可以预见,在不久的将来,自愈合水凝胶生物电子学将融入人类的日常生活,使人们的生活方式发生革命性的变化。
-
电子器件
+关注
关注
2文章
595浏览量
32167 -
水凝胶
+关注
关注
0文章
26浏览量
9133 -
触觉传感
+关注
关注
0文章
11浏览量
8246
原文标题:综述:自愈合水凝胶生物电子器件研究进展
文章出处:【微信号:Micro-Fluidics,微信公众号:微流控】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
碳基射频电子器件的研究进展

CBM24AD99Q | 重塑生物电势测量,开启精准医疗新时代

同济大学:研究基于双极性驻极体的全生物可降解、高灵敏度压力传感器及体内/外生物力学信号监测应用
AI大模型的最新研究进展
生物电信号的主要的基本有哪些
电压驱动的电力电子器件有哪些
导热纸(膜)的研究进展 | 晟鹏技术突破导热芳纶纸

综述:高性能锑化物中红外半导体激光器研究进展

综述:基于微流控技术的氧释放生物材料的制备与应用研究进展




 综述:自愈合水凝胶生物电子器件研究进展
综述:自愈合水凝胶生物电子器件研究进展












评论