原电池通过化学反应产生电流,其工作原理涉及到氧化还原反应,即一个物质失去电子(氧化),而另一个物质获得电子(还原)。在原电池中,阳离子和阴离子的移动对于维持电流的流动至关重要。盐桥的使用在双液原电池中尤为重要,它的作用是保持电解质溶液的电中性,从而确保电池的有效运行。以下是对盐桥作用的详细分析:
1. 电中性的维持
在原电池工作时,一个半电池中的阳离子会向该半电池的电极移动,参与氧化还原反应。这会导致该半电池的电解质溶液失去阳离子,从而带负电荷。盐桥作为连接两个半电池的桥梁,允许其内部的阳离子迁移到带负电荷的电解质溶液中,以维持电中性。
2. 电荷平衡
盐桥内部通常填充有高浓度的电解质,这些电解质不参与电池的氧化还原反应,但它们的阳离子可以自由移动。当一个半电池失去阳离子时,盐桥中的阳离子会补充进来,保持了整个电池系统的电荷平衡。
3. 电流的持续流动
由于盐桥的介入,即使在两个半电池的电解质溶液中存在不同的化学物质,电子也能够通过外部电路从一个半电池流向另一个半电池,形成闭合回路,使电流得以持续流动。
4. 防止溶液混合
在双液原电池中,盐桥的使用还防止了两个半电池的电解质溶液混合,这种混合可能会引起不希望的化学反应,导致电池性能下降或失效。
5. 电池的极化现象减少
电池在工作时,电极表面的离子浓度可能会与溶液主体中的离子浓度出现显著差异,这种现象称为极化。盐桥的使用有助于减少极化现象,因为它能够及时补充或移除离子,以维持电极表面的离子浓度。
6. 提高电池效率
由于盐桥能够维持电中性并减少极化,它有助于提高电池的整体效率。电池能够更有效地将化学能转化为电能,而不会因为离子浓度的不均衡而损失能量。
7. 电池的稳定性
盐桥还有助于维持电池的稳定性。在电池放电过程中,可能会出现某些离子的积累或耗尽,这会导致电池性能的不稳定。盐桥通过允许离子的迁移,有效地避免了这种情况的发生。
8. 盐桥的材料选择
盐桥通常由不可燃、不导电但能允许离子通过的材料制成,比如凝胶状的电解质或某些类型的离子交换树脂。这些材料的选择对于盐桥的效能至关重要。
9. 盐桥设计的影响
盐桥的设计,包括其长度、直径和电解质浓度,都会影响电池的性能。设计不当的盐桥可能无法有效维持电中性,导致电池性能下降。
10. 实验观察
通过热成像技术可以观察到双液原电池在工作时发热部位的关键证据,这表明盐桥在电池性能上优于单液原电池,尤其是在最大输出电流和放电效率方面。
结论
盐桥在原电池中发挥着至关重要的作用,它通过允许特定离子的迁移来保持电池中电解质溶液的电中性,从而确保了电池的有效运行和高效率。在设计和使用原电池时,必须仔细考虑盐桥的材料选择和设计,以优化电池性能并确保安全稳定的放电过程。
-
电解质
+关注
关注
6文章
817浏览量
20101 -
原电池
+关注
关注
0文章
48浏览量
7434 -
电池系统
+关注
关注
9文章
390浏览量
29953
发布评论请先 登录
相关推荐
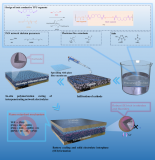
半互穿网络电解质用于高电压锂金属电池




 原电池为何需要盐桥来保持电解质溶液的电中性?
原电池为何需要盐桥来保持电解质溶液的电中性?










评论