心脏是人体中一个复杂而重要的器官,具有心脏毒性的药物如乌头碱等严重制约了其临床应用,建立合适的三维(3D)体外心脏模型有助于探究乌头碱的心脏毒性机制,指导临床安全用药。
通过液滴微流控技术制备的多隔室心脏颗粒模型具有低成本、高灵活性和高通量的特点,是应用于药物心脏毒性机制研究的理想模型。
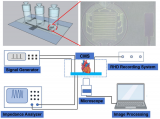
近日,清华大学林金明教授带领研究团队与成都中医药大学张艺教授团队合作,制备了一种具有操作简便、无标记检测和可控性强等特点的六隔室心脏颗粒,并通过液相色谱-质谱联用仪(LC-MS)检测了乌头碱心脏毒性反应下的细胞代谢物,以及利用分子生物学技术评估了乌头碱刺激后心脏毒性相关指标的表达,最后总结了乌头碱的心脏毒性机制。
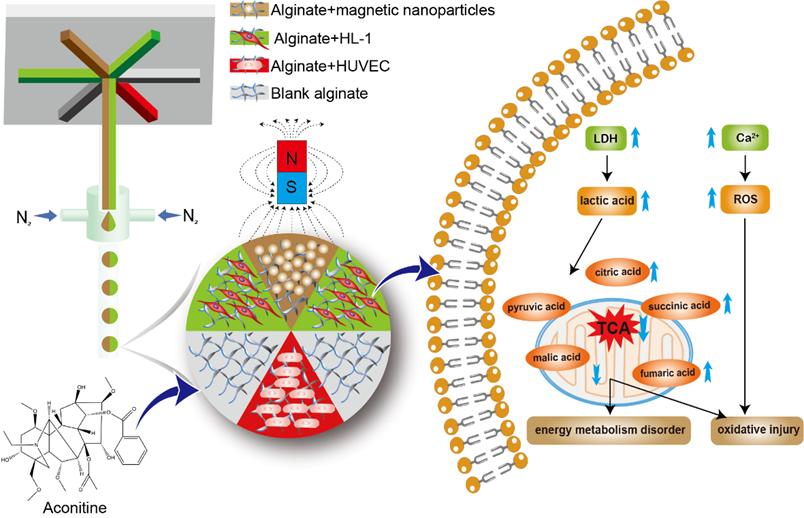
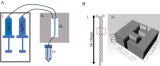
该工作设计的微流控装置制备了由HL-1和HUVEC细胞3D共培养的六隔室心脏颗粒模型,该模型用磁颗粒定位,在不需要标记的情况下能够清楚地观察到每个隔室的细胞状态。此外,研究人员通过LC-MS和分子生物学技术发现乌头碱能够破坏细胞膜结构引起乳酸脱氢酶(LDH)外渗和Ca²⁺超载,从而抑制三羧酸(TCA)循环,导致能量代谢紊乱和氧化损伤,最终引发心肌细胞凋亡。
这些结果提供了一种新型的体外心脏模型以及药物的安全研究策略。该成果以“Evaluation of aconitine cardiotoxicity with aheart-on-a-particle prepared by a microfluidic device”为题,发表在英国皇家化学会期刊ChemicalCommunications上,并入选为hot article。
论文链接:
https://doi.org/10.1039/D4CC00396A
-
色谱仪
+关注
关注
0文章
40浏览量
11499 -
微流控
+关注
关注
16文章
560浏览量
19132
原文标题:3D)
文章出处:【微信号:Micro-Fluidics,微信公众号:微流控】欢迎添加关注!文章转载请注明出处。
发布评论请先 登录
相关推荐
微流控芯片在细胞培养检测中的应用
中国科学技术大学团队突破非接触心脏活动感知技术
电源的“心脏”——充电模块
微流控技术的生物学应用
使用原代肿瘤细胞进行药物筛选的数字微流控系统
高通量生物分析技术之微流控芯片
微流控芯片3大制作技术
激光焊接技术在焊接医疗心脏射频消融导管的工艺应用

综述:基于微流控技术的氧释放生物材料的制备与应用研究进展




 利用微流控技术制备的“心脏颗粒”,用于评估药物的心脏毒性
利用微流控技术制备的“心脏颗粒”,用于评估药物的心脏毒性












评论