传感新品
【中国科学院大学:实现可再生高灵敏度生物传感器新进展】
可再生的即时检测(POC)传感器为疾病标志物的快速检测提供了一类新型解决方案,但是该类器件面临循环使用过程中重复污染难题,难以兼具高灵敏度和优异的循环使用次数,制约了该领域的快速发展。
中国科学院大学张凤娇副教授、中国科学院大学/中国科学院化学研究所狄重安研究员与中国人民解放军总医院李佳副主任医师报道提出药物分子探针介导的有机电化学晶体管(DM-OECT)构建新思路,器件对血液中的血液表皮生长因子(EGFR)具有高灵敏检测能力,同时具有独特的可再生功能,为POC传感器的低成本制备提供了新思路。
POC传感器可实现疾病标志物的快速检测,是重大疾病诊疗和术后康复监测的重要路径,也是生物电子学的重要发展方向之一。然而,现有的POC传感器普遍成本较高,且特定疾病需要长期高频率检测,为高风险人群带来了巨大的经济负担。可再生POC传感器的核心特征是利用单个器件实现标志物的多次灵敏检测,进而大幅降低使用成本。传统的再生方式是通过pH调控、加热或施加电压诱导探针与待测物的结合发生解离,但热动力学平衡和可逆吸附会造成表面反复污染,使得器件在循环使用过程中灵敏度快速下降。利用物理或化学刻蚀方法可以避免物质残留,但会破坏活性层进而限制器件循环使用次数的提高。
在这项工作中,研究人员提出了全新的药物分子探针介导的有机电化学晶体管传感器(DM-OECT)理念(图1)。该器件具有“refresh-in-sensing(传感中再生,RIS)”的新机制,即器件在待测物检测过程中实现同步再生。研究人员使用吉非替尼药物分子为探针,利用吉非替尼与有机半导体的电荷转移、吉非替尼与EGFR的特异性靶向作用、EGFR-吉非替尼的构象翻转,实现EGFR的高灵敏度传感以及传感过程中的功能表面再生。
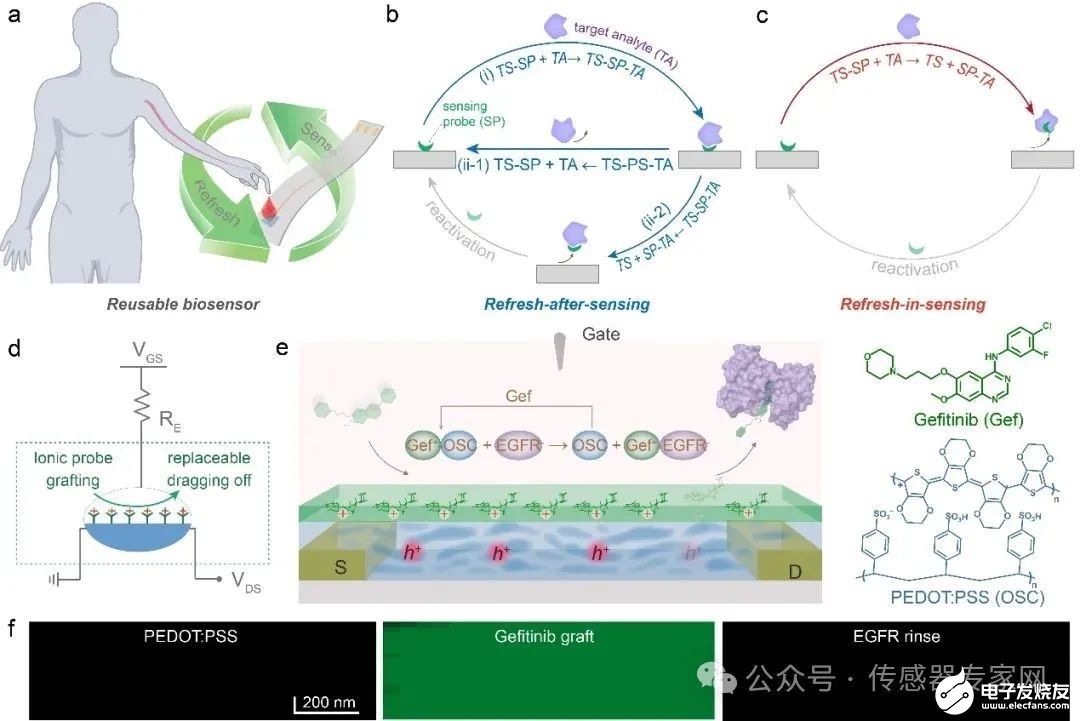
图1:DM-OECT可再生传感器示意图与拉曼成像图。
利用该类器件,研究团队成功实现了血液表皮生长因子EGFR的灵敏检测,其检测极限降低了两个量级,可以达到fg/mL(图2)。更为重要的是,该类器件可以实现超过200次的重复高灵敏检测(图3),且稳定性超过28周,满足血液生物标志物的低成本、长周期监测需求。研究还通过多种活性层、药物探针和待测物验证了该方法的普适性。
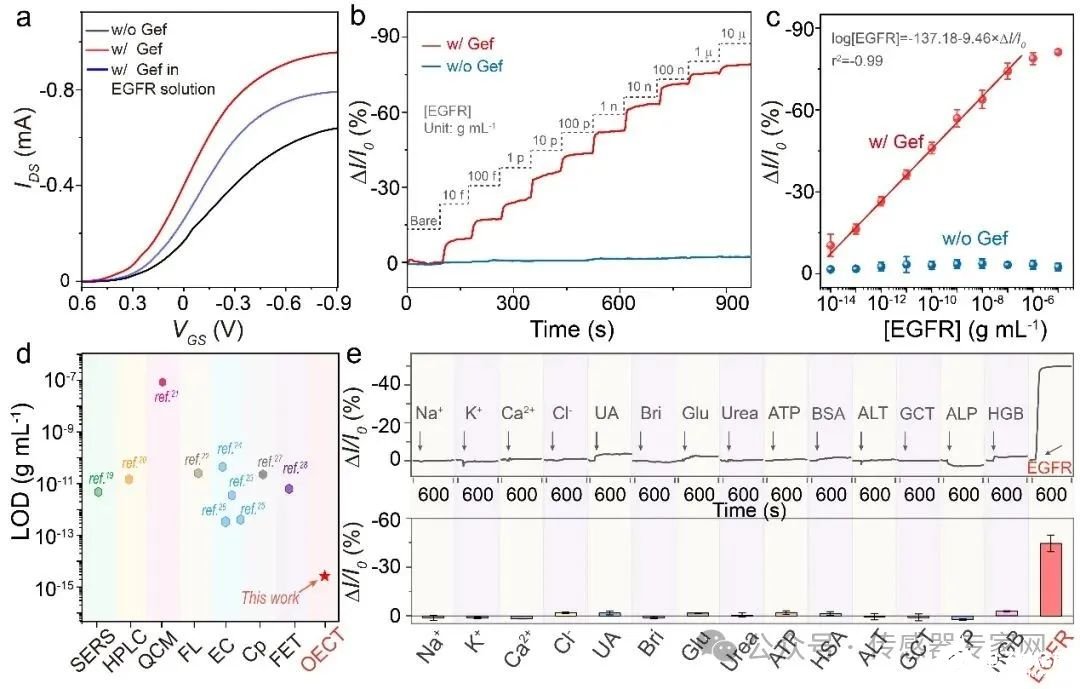
图2:基于DM-OECT的EGFR传感表征结果。
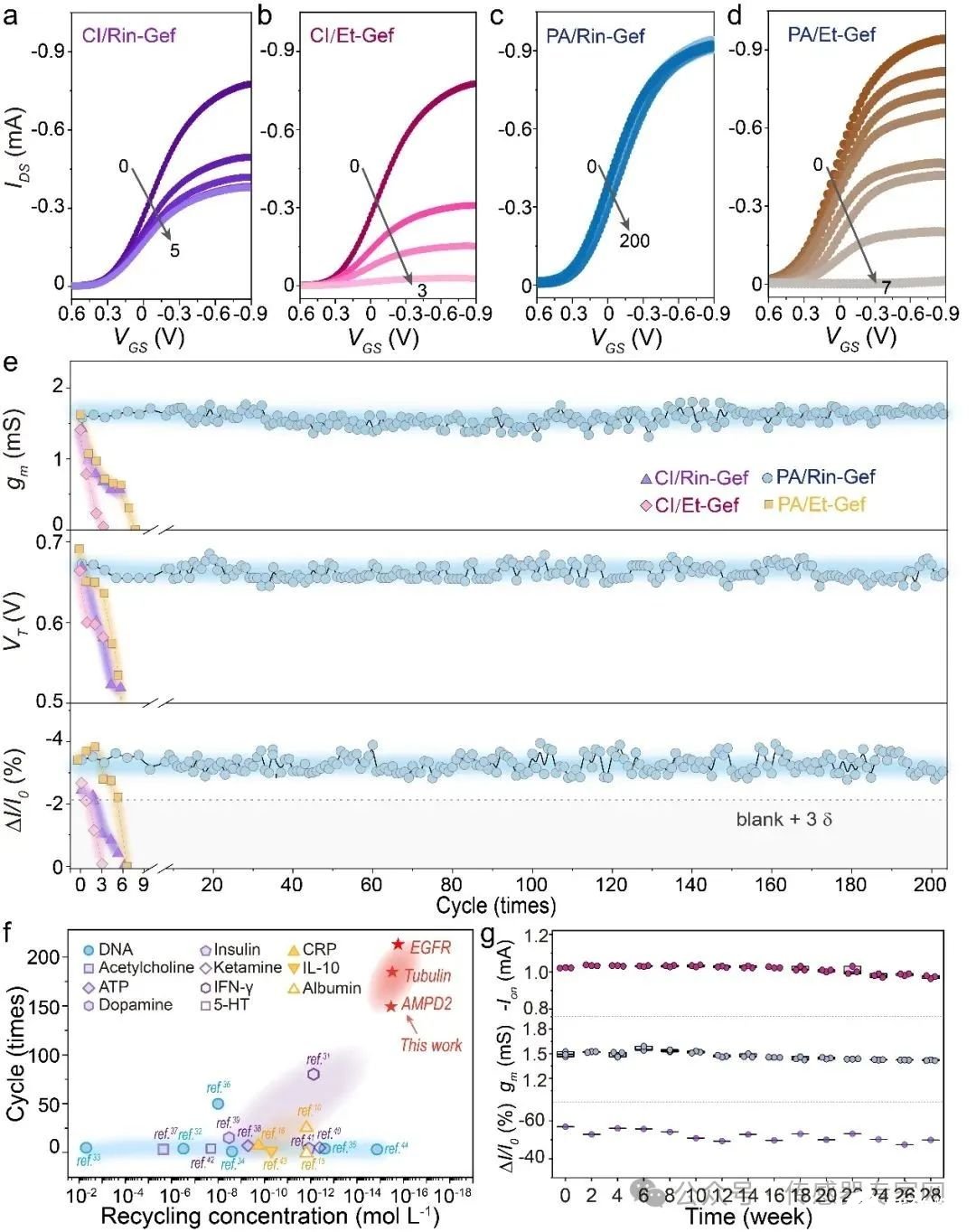
图3:DM-OECTs的可再生性能表征结果。
研究团队结合系列界面表征技术,揭示了药物分子探针介导的RIS传感机制(图4)。对于有机电化学晶体管,吉非替尼靠近时与PEDOT:PSS发生电荷转换,通过质子化改变表面电位,降低电解质与半导体界面处电势,增强了半导体层的导电性。当EGFR靠近探针层表面,其强结合作用与构型翻转特性将吉非替尼分子拽离PEDOT:PSS表面,通过去质子化降低器件电流,完成RIS过程。
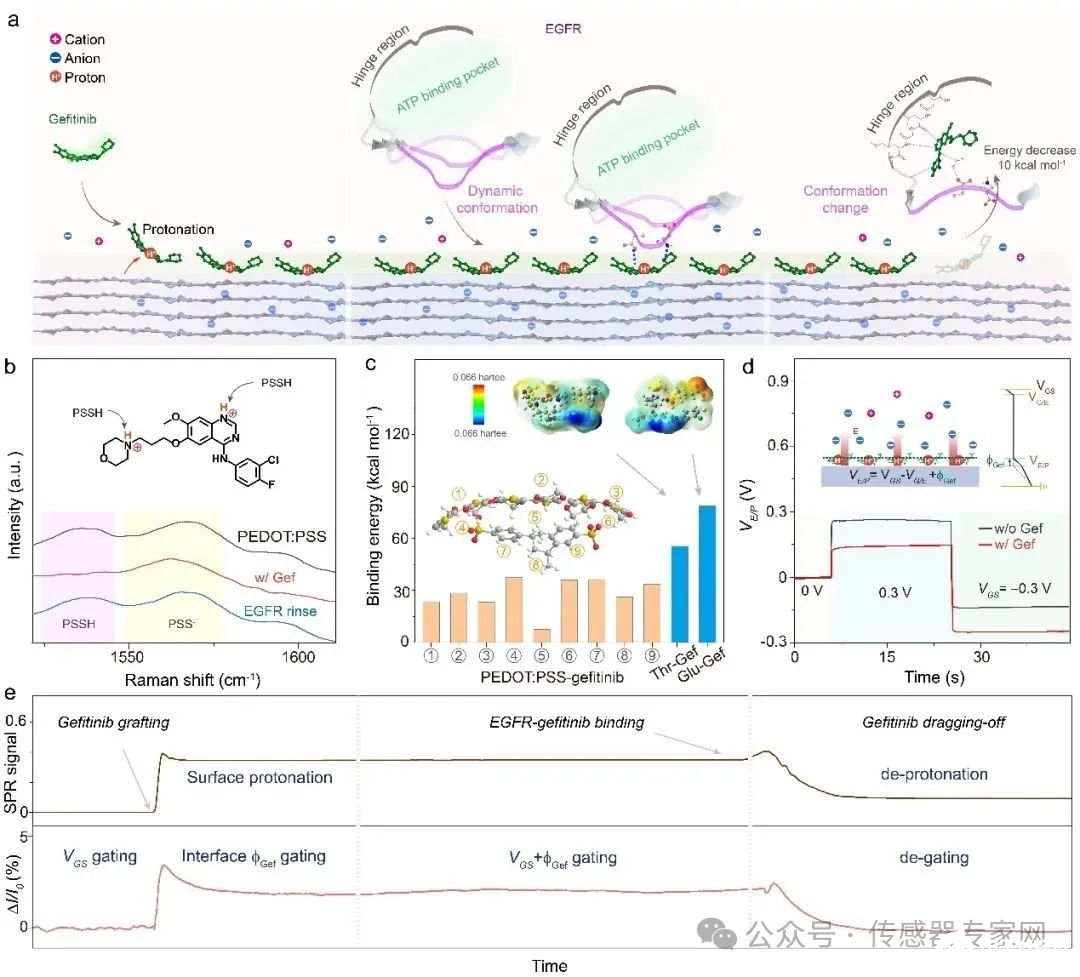
图4:DM-OECT的RIS传感机制。
在此基础上,研究团队开发了便携式血液测试盒,展示了用于非小细胞肺癌(NSCLC)患者EGFR定量分析的阵列器件(图5)。该器件在全血中保持了可再生高灵敏度传感性能,循环使用前后均可有效地区分健康个体和NSCLC患者的血液EGFR水平的差异,其主要性能指标可以媲美酶联免疫吸附试验试剂盒。更为重要的是,该方法有望将检测成本降低一个量级以上,为EGFR的低成本连续监测提供了有效方法。
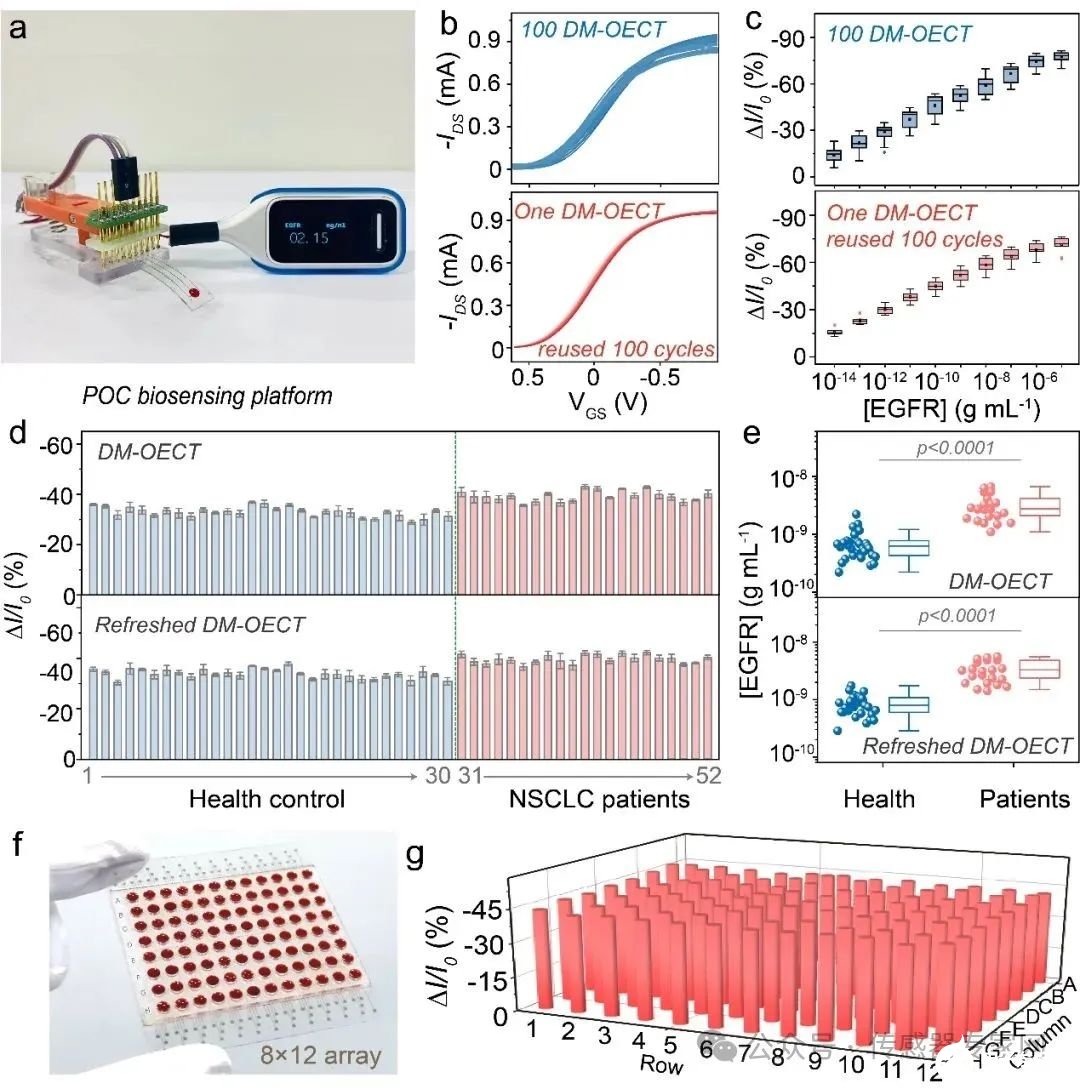
图5:可再生DM-OECT的临床血液检测结果。
总之,研究人员提出了药物分子介导有机电化学传感器设计新策略,为新型有机生物电子器件构筑及其相关的POC生物医学应用提供了新思路。
原文链接 https://doi.org/10.1038/s41563-024-01970-5
声明:转载此文是出于传递更多信息之目的,若有来源标注措误或侵犯了您的合法权益,请与我们联系,我们将及时更正、删除,谢谢。
-
生物传感器
+关注
关注
12文章
374浏览量
37443
发布评论请先 登录
相关推荐
高检测灵敏度的DNA 生物传感器介绍
高灵敏度薄膜生物传感器基因芯片系统的研制
超高灵敏度石墨烯太赫兹探测器研究获突破

高灵敏度薄膜生物传感器应用
中国科学院在薄膜太阳能电池材料的研究方面取得新进展
西安推出超高灵敏半导体光电生物传感器 实现对蓝藻缓慢生长期的探测
中国农大:在生物传感器方面研究取得新进展,具有现场检测食源性致病菌的潜力
中国科学院天津工业生物技术研究所:在基于转录调控因子的生物传感器研究方面取得进展
中国科学院西安光学精密机械研究所与西北大学:表面功能化光纤传感器研究获进展
中国科学院:金属所柔性应变传感器的手势识别应用研究取得进展
中国科学院在薄膜荧光传感器研究方面取得进展,美国为F-22升级新传感器

中国科学院西安光机所智能光学显微成像研究取得新进展





 中国科学院大学:实现可再生高灵敏度生物传感器新进展
中国科学院大学:实现可再生高灵敏度生物传感器新进展










评论