克容量是指电池电极活性物质中的锂离子全部参与电化学反应所能释放出的电容量与活性物质的质量之比。
克容量是针对电池活性物质的概念,电池活性物质包括:可做正极材料的钴酸锂、磷酸铁锂、锰酸锂等,可做负极材料的石墨。
克容量可以被理解为每克活性物质所含的电容量,通常克容量单位是毫安时每克(mAh/g)。有时克容量也可被称为比容量。
电荷量和法拉第常数是理论克容量相关的两个概念。
电荷量表示电荷的多少,单位是库仑(C)。如果导线载有1安培(A)的稳定电流,则在1秒内通过导线横截面积的电量为1库仑(C),根据上述定义,可得出如下公式:
1A×1s=1C
根据1A=1000mA,1s=1/3600h,可以得出:
1mAh=3.6C

图片来源:学堂在线《锂离子电池材料与技术》
法拉第常数(F)是指每摩尔电子所携带的电荷量,单位是C/mol。法拉第常数等于阿伏伽德罗常数(1摩尔的粒子个数,NA=6.02214×1023mol-1)与元电荷电量(e=1.602176×10-19C)之积。经计算,法拉第常数等于96485C/mol。

图片来源:学堂在线《锂离子电池材料与技术》
在锂离子电池中,一个锂离子对应一个电子,锂离子和电子所携带的电荷量相等。
下文以钴酸锂(LiCoO2)为例计算理论克容量:
钴酸锂(LiCoO2)的摩尔质量是97.8728g/mol(可根据Li、Co、O的相对原子质量加和近似得出。)
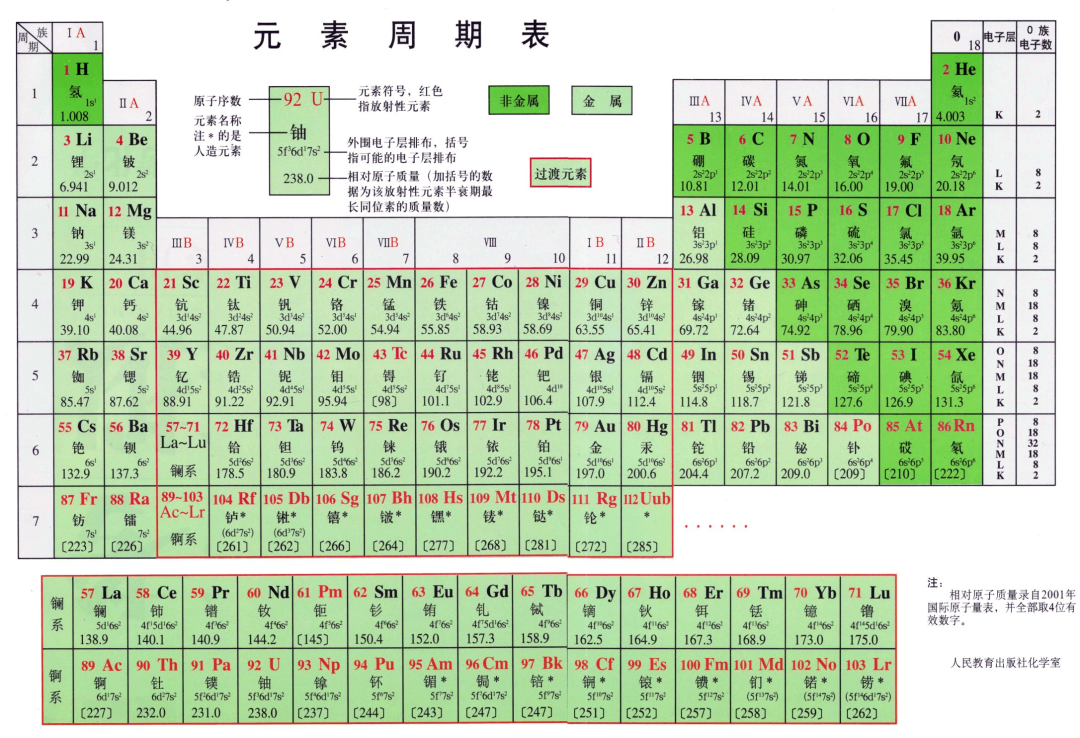
图片来自网络
则1g钴酸锂(LiCoO2)物质的量(物质的量是表示物质含有粒子数的量,符号为n)。
n=1g/(97.8728g/mol)=0.01021734332mol
则1g钴酸锂(LiCoO2)提供电荷量等于钴酸锂(LiCoO2)物质的量乘以法拉第常数,即:
0.01021734332mol×96485C/mol=985.82C
换算成mAh为单位表示:
985.82/3.6=274mAh
即钴酸锂(LiCoO2)材料的理论克容量为274mAh/g。
总结以上计算过程,得出如下公式:
理论克容量=(1/摩尔质量)×Li计量个数×法拉第常数×(1/3.6)
个人理解:Li计量个数表示材料容纳最多数量的锂原子时的化学式中可移动锂元素的个数。摩尔质量表示材料容纳最多数量的锂原子时,化学式中各元素相对原子质量之和,正极材料的相对原子质量之和包含可移动的锂元素,负极材料的相对原子质量之和不包含可移动的锂元素。
下文计算磷酸铁锂(LiFePO4)正极材料、石墨负极材料、硅负极材料的理论克容量:
(1)磷酸铁锂正极材料
磷酸铁锂(LiFePO4)的摩尔质量为157.756g/mol,根据理论克容量公式计算:
理论克容量=(1/157.756)×1×96485×(1/3.6)=170mAh/g
即磷酸铁锂(LiFePO4)正极材料的理论克容量为170mAh/g。
(2)石墨负极材料
石墨(C)负极中,当锂嵌入量最大时,形成锂碳层间化合物,化学式为LiC6,即6个碳原子结合一个锂原子。六个碳(C)的摩尔质量为72.066g/mol(不包含可移动的锂元素),根据理论克容量公式计算:
理论克容量=(1/72.066)×1×96485×(1/3.6)=372mAh/g
即石墨负极材料的理论克容量为372mAh/g
(3)硅负极材料 硅作为电池负极时,与锂发生如下合金化反应:
5Si+22Li++22e-Li22Si5
生成的产物为Li22Si5,5个硅的摩尔质量为140.4g/mol(不包含可移动的锂元素),5个硅原子结合22个锂原子,因此硅负极材料的理论克容量为:
理论克容量=(1/140.4)×22×96485×(1/3.6)=4200mAh/g
审核编辑:刘清
